题目内容
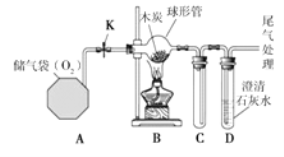
【题目】用右图所示装置测定空气中氧气的含量,其中集气瓶的容积为200 mL,量筒的容量为250 mL。实验步骤如下(装置气密性良好):

I.打开止水夹a和b,向集气瓶中缓慢鼓入一定量空气,稍后,测得进入到量筒中的水的体积为V1mL;
II.用强光手电照射,引燃红磷;
III.红磷熄灭并冷却至室温,打开止水夹b,测得量筒中的水的体积变为V2mL;
IV.计算空气中氧气的体积分数。
(1)红磷燃烧的化学方程式为___________________。
(2)整个实验过程中的现象为___________________________________。
(3)步骤Ⅱ中引燃红磷前应进行的操作是___________________,否则会影响测定结果。
(4)步骤III中,未冷却至室温会使测得的V2数值___________(填“没有影响”、“偏高”或“偏低”)。
【答案】(1)4P+5O2点燃2P2O5(2)鼓入空气时集气瓶中大部分水排入量筒中,红磷燃烧产生大量白烟,冷却后打开b,量筒中的水进入集气瓶中(3)关闭止水夹a和b (4)偏高
【解析】
试题分析:(1)红磷燃烧生成的是五氧化二磷:4P+5O2点燃2P2O5;
(2)鼓入空气时,压强变大,集气瓶中大部分水排入量筒中;红磷燃烧产生大量白烟,冷却后打开b,由于集气瓶中的压强变小,量筒中的水进入集气瓶中;
(3)点燃红磷前要关闭止水夹,否则空气会进入导致实验结果不准确;
(4)步骤III中,未冷却至室温就打开止水夹,由于集气瓶中压强变化不大,会导致进入集气瓶中的水偏少,即V2数值偏大。

练习册系列答案
相关题目