题目内容
【题目】某化学兴趣小组在用铜丝和银丝做实验时,发现久置的铜丝表面能生成绿色的铜锈,兴趣小组对铜生锈的条件进行了以下探究。
(查阅资料)铜锈的主要成分为Cu2(OH)2CO3。
(作出猜想)铜生锈可能与空气中的氧气有关外,还可能与_____有关,作出此猜想的依据是_____。
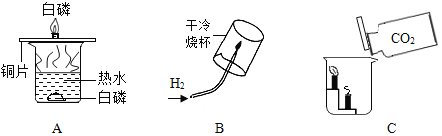
(实验设计)兴趣小组同学取4根铜丝设计了如下图所示的四个实验。
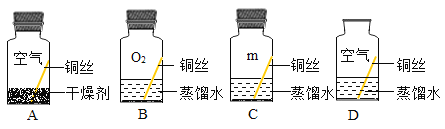
他们为了除去铜丝表面的污物,实验前应该做的操作是_____。C瓶中的m应该是_____。
(现象分析)若干天后,发现只有D瓶中的铜丝表面出现绿色的铜锈,其他瓶中的铜丝表面均无铜锈出现。
(1)实验B、C瓶中所使用的蒸馏水是经煮沸后迅速冷却的蒸馏水,其目的是_____。
(2)通过B瓶与D瓶中的现象对比,可以得出铜生锈与_____有关的结论。
(实验结论)由上述四个实验可以分析得出猜想成立,写出铜生锈的化学方程式_____。
(讨论交流)在同样环境下银丝依旧光亮如新,原因是_____。
【答案】二氧化碳、水 根据质量守恒定律,化学反应前后元素种类不变 用砂纸打磨 二氧化碳 除去蒸馏水中的氧气 二氧化碳 2Cu+O2+CO2+H2O=Cu2(OH)2CO3 银的金属活动性比铜弱,不易与氧气反应
【解析】
对比实验AD可知铜生锈与水有关,对比实验BD可知铜生锈与二氧化碳有关,对比实验CD可知铜生锈与氧气有关,由上述四个实验可以得出铜生锈与空气中和氧气、二氧化碳和水有关。
[作出猜想]由于铜绿[化学式为Cu2(OH)2CO3],根据质量守恒定律,铜生锈一定是与含碳、氢、氧的物质发生反应,结合空气的组成,提出合理猜想:铜生锈的条件是铜与氧气、水、二氧化碳同时接触。
故填:二氧化碳、水;根据质量守恒定律,化学反应前后元素种类不变;
[实验设计]
他们为了除去铜丝表面的污物,实验前应该做的操作是用砂纸打磨;铜生锈的条件可能是铜与氧气、水、二氧化碳同时接触,C瓶中的m应该是了二氧化碳。
故填:用砂纸打磨;二氧化碳;
(1)实验B、C瓶中所使用的蒸馏水是经煮沸后迅速冷却的蒸馏水,其目的是除去蒸馏水中的氧气。
故填:除去蒸馏水中的氧气;
(2)B中含有氧气、水,没有二氧化碳,D中含有氧气、水和二氧化碳,铜生锈是否需要空气中的二氧化碳,变量是有二氧化碳,其余条件必须相同,所以B和D形成对照实验,可以探究是否需要有二氧化碳参加反应,故得出结论:铜生锈需要二氧化碳。
故填:铜生锈需要二氧化碳;
[实验结论]由上述四个实验可分析得出,铜生锈是铜与空气中的氧气、水和二氧化碳共同作用的结果,铜生锈的化学方程式为:2Cu+O2+CO2+H2O=Cu2(OH)2CO3。
故填:2Cu+O2+CO2+H2O=Cu2(OH)2CO3;
[讨论交流]在同样环境下银丝依旧光亮如新,原因是:银的金属活动性比铜弱,不易与氧气反应。
故填:银的金属活动性比铜弱,不易与氧气反应。

 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案