��Ŀ����
����Ŀ����������������벻���������ϣ����ſƼ�ˮƽ�IJ�����ߣ���������Ͻ����ճ������а�����Խ��Խ��Ҫ�Ľ�ɫ��
��1������ʱ���й����ϵ�ұͭ�����ǡ�ʪ��ұͭ����Ҫ�ķ�Ӧԭ������������ͭ��Һ��Ӧ��д����Ӧ�Ļ�ѧ����ʽ_____��
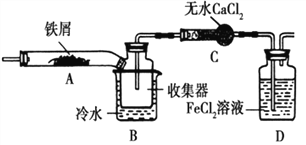
��2�������������������г��õĴ��ߣ���ͼ��������ʾ��ͼ��
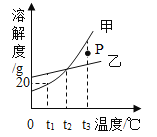
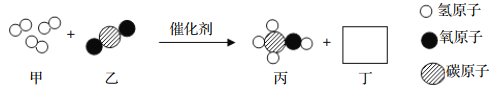
���������е��л��ϳɲ�����_____������д���ƣ���
������ʱ�����е����Ż���ù��Ǹ�����ԭ����_____��
��ͭҲ�����⣬ͭ�����Ҫ�ɷ��Ǽ�ʽ̼��ͭ��Cu��OH��2CO3������ͭ������е�������ˮ��_____��ͬ���õĽ����
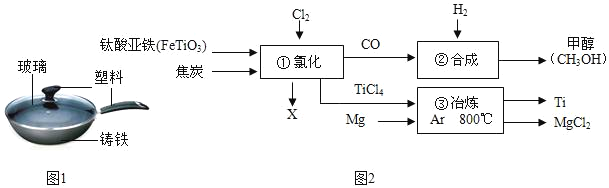
��3���Ѻ��ѺϽ���Ϊ��21���͵���Ҫ�������ϣ����㷺���ڻ��������������ɻ��������ȣ���ͼΪij������ҵ����������ʾ��ͼ��
��ش��������⣺
��FeTiO3����Ԫ�صĻ��ϼ�Ϊ_____��
���Ȼ��л�ѧ����ʽΪ2FeTiO3+6C+7Cl2![]() 2C+2TiCl4+6CO2����XΪ_____���ѧʽ����
2C+2TiCl4+6CO2����XΪ_____���ѧʽ����
���ϳ���CO��H2�Ի�ѧ������1��2ǡ����ȫ��Ӧ����÷�Ӧ�Ļ�����Ӧ������_____��
��ұ���������������_____���ò���Ӧ�Ļ�ѧ����ʽΪ_____��
���𰸡�Fe+CuSO4��FeSO4+Cu ���� �������� ������̼ +4 FeCl3 ���Ϸ�Ӧ ������ 2Mg+TiCl4![]() Ti+2MgCl2
Ti+2MgCl2
��������
��1����������ͭ��Ӧ��������������ͭ����ѧ����ʽΪ��Fe+CuSO4��FeSO4+Cu��
��2���� ���������ǽ������ϣ������ǽ������ϣ��������е��л��ϳɲ��������ϣ�
�� ����ʱ�����е����Ż���ù��Ǹ�����ԭ���ǣ�����������
�����������غ㶨�ɿ�֪��ͭ������ͭ������е�������ˮ�Ͷ�����̼��ͬ���õĽ����
��3������FeTiO3�У���Ԫ����+2�ۣ���Ԫ����ʾ��2�ۣ��裺��Ԫ�صĻ��ϼ�Ϊx��+2+x+����2����3��0��x��+4��������Ԫ�صĻ��ϼ�Ϊ+4�ۣ�
����ѧ��Ӧǰ��Ԫ���������䣬��Ӧ����2����ԭ�ӣ�2����ԭ�ӣ�6����ԭ�ӣ�6��̼ԭ�ӣ�14�������ӣ�����������2����ԭ�ӣ�8����ԭ�ӣ�6��̼ԭ�ӣ�6����ԭ�ӣ�����X��FeCl3��
��CO��H2�Ի�ѧ������1��2ǡ����ȫ��Ӧ������CH3OH���÷�Ӧ����������������һ�����ʣ�������Ӧ�����ǻ��Ϸ�Ӧ��
��ϡ������Ļ�ѧ�����ȶ�����������������þ�����Ȼ�����800��������������Ѻ��Ȼ�þ����ѧ����ʽΪ��2Mg+TiCl4![]() Ti+2MgCl2��
Ti+2MgCl2��

 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д�����Ŀ������ʯ��ʯ����Ҫ�ɷ� CaCO3��������ʯ�ң�CaO���Ͷ�����̼��Ϊ�˲ⶨijʯ��ʯ��̼��ƣ�CaCO3���ĺ������ֳ�ȡ 24.0g ʯ��ʯ��Ʒ�������Ĵθ������ա���ȴ������ʣ���������� �����ʲ��μӷ�Ӧ������¼ʵ���������£�
���� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
ʣ��������� | 21.6g | 19.2g | 15.2g | 15.2g |
�Լ��㣺
��1����ȫ��Ӧ�����ɶ�����̼������Ϊ_____��
��2�����ʯ��ʯ��Ʒ��̼��Ƶ�����_____��