��Ŀ����
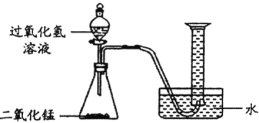
����Ŀ��ijͬѧ��100.00gˮ�м���0.56g������(����ͼA)��������˺���ʵ�鷽����
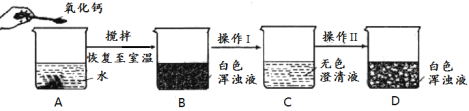
(1)�����Ƶ��׳���___________��
(2)A�з����ķ�Ӧ�Ļ�ѧ����ʽΪ___________��
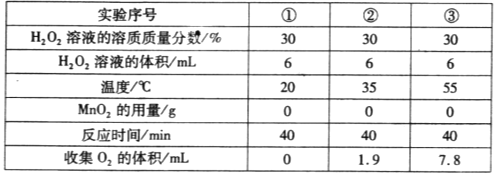
(3)�������£���B�а�ɫ����Һ��ΪC����ɫ����Һ��������I����������_________��
(4)���C��Һ��������Ϊ100.00g�����������ʵ���������Ϊ______(������λС��)��
(5)�����IIΪͨ��һ�����壬������Ӧ�Ļ�ѧ����ʽΪ __________��
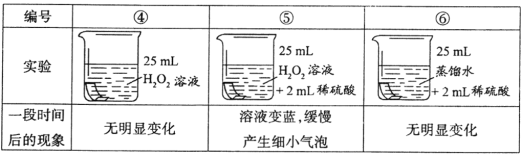
(6)�����IIΪ��������ij���壬��ù��������_______(�����)��
�������� �ڱ��� ���Ȼ��� ����������
���𰸡���ʯ�� CaO+H2O�TCa��OH��2 ���� 0.18% Ca��OH��2+CO2�TCaCO3��+H2O �٢�
��������
��1���������׳���ʯ�ң�
��2����������ˮ��Ӧ�����������ƣ���Ӧ�Ļ�ѧ����ʽΪ��CaO+H2O�TCa��OH��2��
��3�������Һ���е������Թ�����ù��˲�����
��4�����������Ƶķ�Ӧ��ˮ������Ϊx����

![]()
x=0.18g��
���C��Һ��������Ϊ100.00g����������Һ���������Ƶ�����Ϊ0.18g�����������ʵ���������Ϊ![]() ��100%=0.18%��
��100%=0.18%��
��5�����������������̼��Ӧ����̼��ư�ɫ������ˮ������ͨ�������̼������ǣ���Ӧ�Ļ�ѧ����ʽΪ��Ca��OH��2+CO2�TCaCO3��+H2O��
��6���������Ƶ��ܽ�������¶ȵ����߶���С�������IIΪ��������ij��������ǣ�˵������ù��������ˮ����ˮ��Ӧ�ų�������

 ѧϰʵ����ϵ�д�
ѧϰʵ����ϵ�д�����Ŀ��������ͬѧ�ӡ��Ʊ�����������չ��̽��ʵ������ȡ����IJ���װ������ͼ��ʾ������±����ݡ�
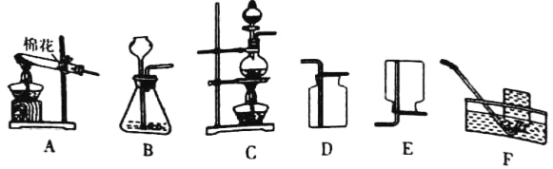
�� �� | ������O2�� | |
ҩ Ʒ | ������� | �������ƣ�CaO2����ˮ |
��Ӧԭ�� ���û�ѧ����ʽ��ʾ�� | _________ | ________ |
ҩƷ״̬����Ӧ���� | _________ | �����Һ�塢���� |
����װ�� | A | _________�����ţ� |
�ռ�װ�� | F��_________�����ţ� | |
���������� ���������ռ���Ϊ���� | ����ʹ�ô����ǵ�ľ����������ͬ��Ϊ_______ | |