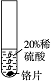
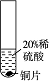
题目内容
某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组进行了如下实验,在一定的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定.
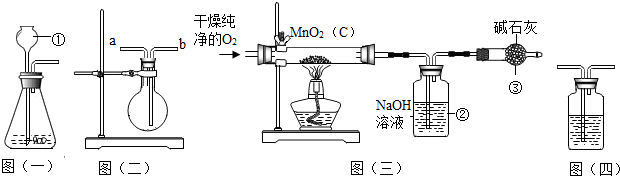
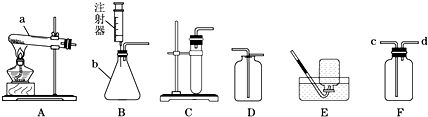
(1)该实验可选择图(一)装置来产生所需氧气.如果要产生平稳的氧气气流,可将仪器①换成 .
(2)用图(二)装置收集或干燥氧气.若在烧瓶内装入浓硫酸来干燥,则气体应从 端通入.
(3)装置③中装有碱石灰,其作用是 .
(4)为了验证装置②已将CO2吸收完全,可在装置②和装置③之间加入图(四)装置进行证明,则图(四)中加入的试剂是 .
(5)称取5.0g二氧化锰样品进行试验,图(三)玻璃管中的前后质量差为1.1g,则样品中的二氧化锰的质量分数为 .
(6)实验完成后,待图(三)玻璃管中的固体冷却至室温后,将该固体投入到过氧化氢溶液中,立即有大量的气泡产生,写出该反应的方程式:
.

(1)该实验可选择图(一)装置来产生所需氧气.如果要产生平稳的氧气气流,可将仪器①换成
(2)用图(二)装置收集或干燥氧气.若在烧瓶内装入浓硫酸来干燥,则气体应从
(3)装置③中装有碱石灰,其作用是
(4)为了验证装置②已将CO2吸收完全,可在装置②和装置③之间加入图(四)装置进行证明,则图(四)中加入的试剂是
(5)称取5.0g二氧化锰样品进行试验,图(三)玻璃管中的前后质量差为1.1g,则样品中的二氧化锰的质量分数为
(6)实验完成后,待图(三)玻璃管中的固体冷却至室温后,将该固体投入到过氧化氢溶液中,立即有大量的气泡产生,写出该反应的方程式:
考点:实验探究物质的组成成分以及含量,气体的干燥(除水),实验室制取氧气的反应原理,碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据发生装置的选择条件即可.
(2)干燥就意味着是浓硫酸,因为浓硫酸具有吸水性.
(3)由题目信息(使杂质炭在加热条件下反应生成CO2来进行分析测定)可知,二氧化碳的测定对实验很重要.因为空气也有二氧化碳.所以要消除空气中二氧化碳对实验的影响.
(4)检验二氧化碳常用试剂就是澄清石灰水.
(5)利用化学方程式进行计算,代入质量分数的计算公式即可.
(6)过氧化氢在二氧化锰的催化作用下生成水和氧气,写出反应的化学方程式即可.
(2)干燥就意味着是浓硫酸,因为浓硫酸具有吸水性.
(3)由题目信息(使杂质炭在加热条件下反应生成CO2来进行分析测定)可知,二氧化碳的测定对实验很重要.因为空气也有二氧化碳.所以要消除空气中二氧化碳对实验的影响.
(4)检验二氧化碳常用试剂就是澄清石灰水.
(5)利用化学方程式进行计算,代入质量分数的计算公式即可.
(6)过氧化氢在二氧化锰的催化作用下生成水和氧气,写出反应的化学方程式即可.
解答:解:
(1)该实验可选择图(一)装置来产生所需氧气.如果要产生平稳的氧气气流,可将仪器①换成分液漏斗;
(2)干燥是一个关键词,说明需要填写一种吸水性物质,浓硫酸具有吸水性;故答案为:b;
(3)根据题目信息(在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定)可知,本实验是通过计算二氧化碳的质量测定质量分数的,所以必须排除空气中的二氧化碳的干扰;二氧化碳可以和碱石灰反应;故答案为:防止空气中的二氧化碳进入②中,影响测定结果.
(4)检验二氧化碳常用方法就是通入澄清石灰水,若石灰水变浑浊,说明是二氧化碳.故答案为:澄清石灰水.
(5)根据题干信息可知,图(三)中装置②反应前后的质量差1.1g就是二氧化碳的质量.
设碳的质量是x,
C+O2
CO2
12 44
x 1.1g
即:
=
,得:x═0.3g
碳的质量分数═
×100%═6%;故二氧化锰的质量分数就是94%.
(6)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2
2H2O+O2↑.
故答案为:
(1)分液漏斗;(2)b;(3)防止空气中的二氧化碳进入②中,影响测定结果.
(4)澄清石灰水.(5)94%.(6)2H2O2
2H2O+O2↑.
(1)该实验可选择图(一)装置来产生所需氧气.如果要产生平稳的氧气气流,可将仪器①换成分液漏斗;
(2)干燥是一个关键词,说明需要填写一种吸水性物质,浓硫酸具有吸水性;故答案为:b;
(3)根据题目信息(在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定)可知,本实验是通过计算二氧化碳的质量测定质量分数的,所以必须排除空气中的二氧化碳的干扰;二氧化碳可以和碱石灰反应;故答案为:防止空气中的二氧化碳进入②中,影响测定结果.
(4)检验二氧化碳常用方法就是通入澄清石灰水,若石灰水变浑浊,说明是二氧化碳.故答案为:澄清石灰水.
(5)根据题干信息可知,图(三)中装置②反应前后的质量差1.1g就是二氧化碳的质量.
设碳的质量是x,
C+O2
| ||
12 44
x 1.1g
即:
| 12 |
| 44 |
| x |
| 1.1g |
碳的质量分数═
| 0.3g |
| 5.0g |
(6)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2
| ||
故答案为:
(1)分液漏斗;(2)b;(3)防止空气中的二氧化碳进入②中,影响测定结果.
(4)澄清石灰水.(5)94%.(6)2H2O2
| ||
点评:通过本题使学生学会设计实验测定某种物质的质量分数,并且能够计算质量分数.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
对下列物质在氧气中燃烧的实验现象描述正确的是( )
| A、石蜡在氧气中燃烧时,有水和二氧化碳生成 |
| B、铝箔在氧气中燃烧时,发出耀眼的白光,生成白色固体 |
| C、红磷在氧气中燃烧时,生成一种红色固体 |
| D、铁丝在氧气中燃烧时,火星四射,生成白色固体 |
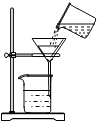 我市某化学兴趣小组的同学用洁净的塑料瓶从釜溪河中取回一定量的水样,然后进行如下研究分析:
我市某化学兴趣小组的同学用洁净的塑料瓶从釜溪河中取回一定量的水样,然后进行如下研究分析: