��Ŀ����
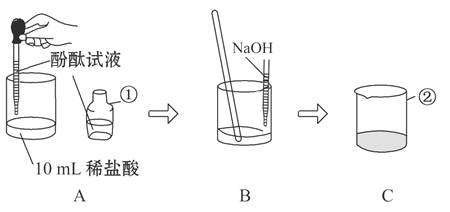
��ͼΪij����ҩ��ʵ��ͼ���ش��������⣮
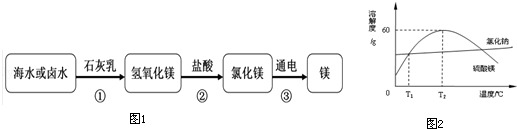
��1��ͼ�б�ʾ�������У����еĽ���Ԫ����������д��һ�ּ��ɣ��������л��ϳɲ��ϵ��������ϡ���
��2��������������������ĸ��ţ���
| A�������� | B������ | C����֬ | D��ά���� |
��4����һ�ֿ���ҩ����Ҫ�ɷ���������þ��Mg2Si3O8?nH2O�����������ᷢ�����ֽⷴӦ����Ӧ������к�þ�Ļ��������� �����ѧʽ����
��1��Al����Ca����2��B��3��ϡ���ᣬ���ݲ�����4��MgCl2
���������������1������ͼʾ���ѿ����������ǽ������ϣ�������Ԫ�أ�̼����к��и�Ԫ�أ��������л��߷��Ӻϳɲ��ϣ��ʴ�Ϊ��Al����Ca����2�����ۡ����ǡ������ǡ���ά�صȶ������࣬�ʴ�Ϊ��B��3������̼�����ܹ�������Һ��Ӧ���ɶ�����̼���壬������ᷴӦ�����κ�ˮ�������������壬��˿�����ϡ�����ϡ����������̼�����ƺ�������þ���ʴ�Ϊ��ϡ���ᣬ���ݲ�����4������������þ�Ǻ�ϡ���ᷢ���ķ�Ӧ�Ǹ��ֽⷴӦ��������ɵ���Ӧ�����Ȼ�������ɵĺ�þ�Ļ�����Ӧ���Ȼ�þ���ʴ�Ϊ��MgCl2
���㣺��Ļ�ѧ���ʣ�̼���ơ�̼��������̼��ƣ�Ԫ�صļ��ࣻ�ϳɲ��ϵ�ʹ�ü�����˺ͻ�����Ӱ�죻�����������Ӫ���أ�

�᷽ܽ����ѧϰ֪ʶ����Ҫ����ͼ��̽���������˶�����Һ�ᡢ���Զ�ͷ����Ӱ�������ʵ�飺
| | �ڲ�ͬPH��Һ�н����� | ||||
| PH="1" | PH=4 | PH="7" | PH=10 | PH=13 | |
| ͷ����� | �ޱ仯 | �ޱ仯 | �ޱ仯 | �� | �ơ����� |
| ͷ��ǿ�� | ���� | ���� | ���� | �� | ���� |
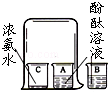
������г������۵�һ�ֳ������ʵİ�װ˵���顣���Ķ��й����ݺش��������⣺
| ��Ҫ�ɷ� | NH4Cl |
| ���淽�� | ������������� |
| ������ | ��25% |
��1��NH4Cl��K2SO4���ǿ�����ѧ���ϵ����ʡ���Ȼ����û�й�ͬ�����Ԫ�أ��������ʣ�������ķ���������ͬ���� �ࣨ��ᡱ����������Ρ��������������
��2����ѧ����ͨ����˵�ġ����������еġ�������ָ ������ţ���
A�������� B����ԭ�� C�������� D����Ԫ��
��3��������������ʵı��淽�����Ʋ�NH4Cl������֮һ ��