题目内容
【题目】根据如图溶解度曲线,下列结论正确的是
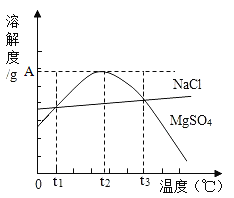
A. NaCl和 MgSO4 的溶解度仅在 t1℃时才相等
B. t2℃时,MgSO4 溶液中溶质质量分数一定大于 NaCl溶液中溶质质量分数
C. t2℃时,升温或降温都可将 MgSO4不饱和溶液变为饱和溶液
D. t3℃时,蒸发少量水一定可使 NaC1 晶体从不饱和溶液中析出
【答案】C
【解析】
A、t1℃和t3℃时,NaCl和MgSO4的溶解度相等,该选项说法不正确;
B、t2℃时,MgSO4的饱和溶液中溶质质量分数一定大于NaCl饱和溶液的质量分数,如果是不饱和溶液,则无法比较大小,该选项说法不正确;
C、t2℃时,硫酸镁的溶解度最大,因此升温或降温都可将MgSO4不饱和溶液变为饱和溶液,该选项说法正确;
D、t3℃时,蒸发少量水不一定可使NaC1晶体从不饱和溶液中析出,该选项说法不正确。
故选C。

练习册系列答案
相关题目
【题目】炎热的夏天,在家中可以自制汽水来消暑解热。
(制备材料)1.5g小苏打、1.5g柠檬酸、蔗糖、果汁、凉开水、500 mL饮料瓶
(制备流程)
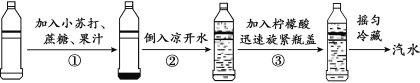
(查阅资料)打开汽水瓶盖,瓶内压强减小,气体的溶解度减小,会有大量气体逸出。喝汽水后会打嗝,因为汽水到胃中后,温度升高,气体的溶解度减小。
(问题讨论)
(1)请结合资料选择Ⅰ或Ⅱ进行解答,若两题均作答,按I计分。
Ⅰ | Ⅱ | |
问题 | 步骤②中为什么要用凉开水制汽水? | 步骤③旋紧瓶盖后,为什么汽水中的气泡会由多变少直至不再冒出? |
答案 | ________ | ________ |
(2)制汽水时,利用了小苏打能与柠檬酸反应产生气体的性质,由此推测下列能与柠檬酸反应的物质有________。
A.镁带 B.铜片 C.食盐 D.纯碱