题目内容
【题目】生活中铜制品放置久了,表面会产生绿色的铜锈。某实验小组分别对铜锈的组成和铜锈蚀的条件进行了探究。
探究1:铜锈由哪些元素组成?
【进行实验】利用下图所示装置对铜锈进行加热,观察到试管口有水珠生成,烧杯中澄清石灰水变浑浊,绿色固体变为黑色。经检测,黑色固体为氧化铜。根据实验,铜锈由__________元素组成。

探究2:铜发生锈蚀的条件是什么?
【查阅资料】亚硫酸钠(Na2SO3)、氢氧化钠可以溶解在水中形成溶液。常温下:亚硫酸钠可与O2发生化合反应;氢氧化钠溶液能吸收CO2。
【猜想与假设】铜的锈蚀可能与O2、CO2、水蒸气有关。
【进行实验】利用如下图装置(铜片长度均为4 cm,试管容积均相同,1和2中未标注的液体为加热后冷却的蒸馏水)进行了5个实验,并持续观察一个月。
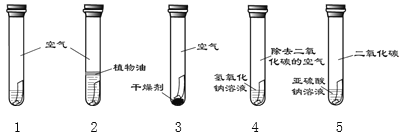
实验现象:只有实验1中铜片小部分发生了锈蚀。
【解释与结论】
(1)实验4的目的是________。
(2)对比实验1和5,得出的结论是________。
(3)由上述实验可推知,铜锈蚀的条件是________。
【反思与评价】
(4)对实验进行反思后,同学们认为实验________可以不用进行。
(5)根据实验结论,请你写出一种防止铜发生锈蚀的方法________。
【答案】 C、H、O、Cu 探究在有O2和H2O无CO2时铜片能否生锈 铜生锈与氧气有关 O2、H2O、CO2同时存在 2 隔绝氧气(或保持干燥或隔绝二氧化碳等)
【解析】(1).由质量守恒定律可知,反应前后元素的种类不变,对铜锈进行加热,观察到试管口有水珠生成,铜锈中有氢、氧元素;烧杯中澄清石灰水变浑浊,证明生成二氧化碳,说明铜锈中有碳元素;绿色固体变为黑色。经检测,黑色固体为氧化铜。证明铜锈中有铜元素。根据实验,铜锈由C、H、O、Cu 元素组成。【解释与结论】(1)实验4中没有二氧化碳时,铜不生锈,证明铜在有O2和H2O无CO2时铜片不生锈。(2)对比实验1和5,试管5内没有氧气不生锈,试管1内有氧气,可生锈,得出的结论是铜生锈与氧气有关。(3)由上述实验可推知,铜锈蚀的条件是O2、H2O、CO2同时存在。【反思与评价】(4)对实验进行反思后,同学们认为实验2可以不用进行。因实验5已经能够证明铜生锈和氧气有关。(5)根据实验结论,可知:铜生锈是铜、氧气、水、二氧化碳四种物质相互作用的结果,所以防止铜发生锈蚀的方法有:隔绝氧气(或保持干燥或隔绝二氧化碳等