题目内容
【题目】请结合图示实验装置,回答下列问题:
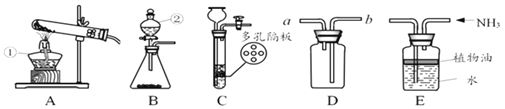
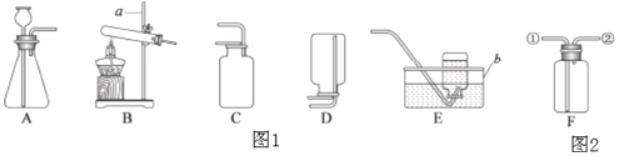
(1)写出有标号的仪器名称:①_____②_____。
(2)用高锰酸钾制氧气选用的发生装置是_____(选填序号),反应的符号表达式为_____,如果选择用D装置收集氧气,气体应从_____通入。
(3)实验室可用B或C装置制CO2,反应的符号表达式为_____,选用C相对于B装置的优点有_____,
(4)实验室可用加热熟石灰与氯化铵的固体混合物的方法制NH3选用的发生装置为_____,用E装置收集氨气,其中植物油的作用是_____。
【答案】酒精灯 分液漏斗 A 2KMnO4![]() K2MnO4+MnO2+O2↑ b CaCO3+2HCl=CaCl2+H2O+CO2↑ 控制反应的开始与结束 A 防止NH3溶于水
K2MnO4+MnO2+O2↑ b CaCO3+2HCl=CaCl2+H2O+CO2↑ 控制反应的开始与结束 A 防止NH3溶于水
【解析】
(1)酒精灯是常用的加热仪器,分液漏斗可以控制反应的速率,故答案为:①酒精灯;②分液漏斗;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;如果选择用D装置收集氧气,气体应从长管进入,因为氧气的密度比空气大;故答案为:A、2KMnO4![]() K2MnO4+MnO2+O2↑、b;
K2MnO4+MnO2+O2↑、b;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,因此不需要加热;选用C相对于B装置的优点有:控制反应的开始与结束;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑、控制反应的开始与结束;
(4)实验室可用加热熟石灰与氯化铵的固体混合物的方法制NH3,因此需要加热;用E装置收集氨气,其中植物油的作用是:防止NH3溶于水;故答案为:A、防止NH3溶于水;

【题目】早在春秋战国时期,我国就开始生产和使用铁器。从1世纪起,铁成了一种最主要的金属材料,工业上可利用一氧化碳还原赤铁矿制得金属铁。
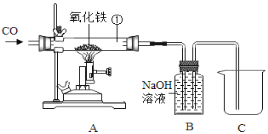
(1)如下图回答问题:
①加热一段时间后玻璃管内的现象是_____,反应的化学方程式为_____
②你认为B装置的优点是_____
(2)工业上可利用“铝热反应”焊接钢轨、冶炼难熔金属等,其原理是在高温下用铝将某些金属从其氧化物中置换出来,在高温下铝与四氧化三铁反应的化学方程式为_____。
(3)向硝酸银、硝酸铜和硝酸锌的混合溶液中,加入一定量的铁粉,充分反应后过滤,向过滤出的固体中滴加稀硫酸,有气体生成,则过滤出的固体中一定有_____.
(4)现有一包黑色固体粉,可能含有炭粉、CuO、Fe3O4中的两种或者三种,某化学兴趣小组通过实验探究其成分。
I提出问题:该黑色固体粉末成分是什么?
II作出猜想:猜想一:混合固体是炭粉、CuO
猜想二:混合固体是炭粉、Fe3O4
猜想三:混合固体是_____(两种物质写不全不给分)
猜想四:混合固体是炭粉、CuO、Fe3O4
III查阅资料:Fe3O4为黑色粉末,能与盐酸反应,含有Fe3+的盐溶液遇到KSCN(硫氰化钾)溶液时变成红色,Fe(OH)2是一种白色沉淀。
IV实验探究:取一定量的固体于试管中,加足量的盐酸,充分反应后有部分固体溶解,过滤,得到滤液A,并对滤液A的成分进行如下探究:
实验操作 | 实验现象 | 实验结论 |
步骤一:取一定量滤液A于试管中,加入足量的铁粉 | 无红色固体析出 | 该固体物质一定没有_____ |
步骤二:又取一定量的滤液A于试管中,加入少量的KSCN(硫氰化钾)溶液 | 溶液变成红色 | 滤液A中还一定含有的物质是_____ |
步骤三:再取一定量的滤液A于试管中,加入足量的NaOH溶液 | 有红褐色沉淀生成,同时还有少量的白色沉淀生成,白色沉淀迅速变成灰绿色,最后面变成红褐色 | 滤液A中还一定含有的物质是_____ |
V讨论交流:
①通过以上实验,猜想_____成立。
②写出Fe3O4与盐酸反应的化学方程式_____。
③Fe3O4与盐酸反应时元素的化合价没有改变,请大家推断Fe3O4中铁元素的化合价为_____(写两种价态才得分)。
VI拓展:请写出同种元素显不同化合价的一种盐_____(其它合理答案也得分)