题目内容
【题目】如图1为实验室用于探究空气中氧气体积分数的常用装置,请回答下列问题:
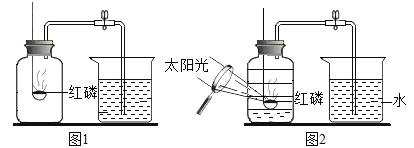
(1)该实验的主要现象:_____。
(2)该反应的文字表达式:_____,该反应的基本类型为_____。
(3)若实验中测得氧气的体积分数高于理论值,则造成此误差的可能原因有哪些?_____(回答一点即可)。
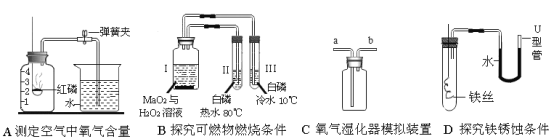
(4)某同学对实验进行反思后,提出了改进方法(如图2所示),你认为改进后的优点是_____。
【答案】产生大量白烟,放热,冷却至室温打开弹簧夹,水被压入集气瓶,约为集气瓶剩余体积的五分之一 红磷+氧气![]() 五氧化二磷 化合反应 弹簧夹没有夹紧(合理均可) 装置严密,误差小
五氧化二磷 化合反应 弹簧夹没有夹紧(合理均可) 装置严密,误差小
【解析】
(1)红磷与氧气反应,生成了五氧化二磷固体,所以会导致集气瓶内压强减小,现象是:产生大量白烟,放热,冷却至室温打开弹簧夹,水被压入集气瓶,约为集气瓶剩余体积的五分之一;故填:产生大量白烟,放热,冷却至室温打开弹簧夹,水被压入集气瓶,约为集气瓶剩余体积的五分之一;
(2)红磷与氧气反应,生成五氧化二磷,该反应的特征是多变一,属于化合反应;故填:红磷+氧气![]() 五氧化二磷;化合反应;
五氧化二磷;化合反应;
(3)若实验中测得氧气的体积分数高于理论值,则造成此误差的可能原因有:弹簧夹没有夹紧,有部分空气在实验过程中逸出或塞橡胶塞过慢,导致集气瓶中空气逸出。故填:弹簧夹没有夹紧;
(4)图2装置设计的比较好,操作简单,并且试管内的空气也不会逸散出来,比较严密;故答案为:装置严密,误差小。

 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案【题目】某兴趣小组对石灰石样品进行如下实验取 12g 样品放入烧杯中,将 100g 稀盐酸分 4 次加入到烧杯中,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下。请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 8 | 4 | 2 | 2 |
求:第 4 次加入稀盐酸后所得溶液中 CaCl2的质量分数。(写出计算过程,最终结果保留 0.1%)。