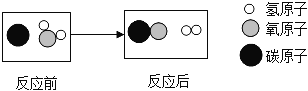
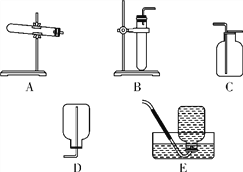
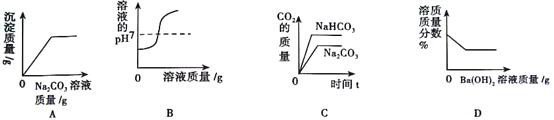
题目内容
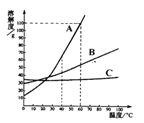
【题目】图1是甲、乙两种固体物质的溶解度曲线。
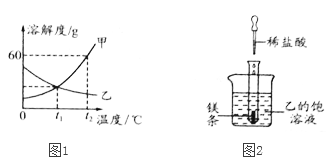
(1)在温度为______℃时,甲、乙两种物质的溶解度相等。
(2)t2℃时,______(填“能”或“不能”)用60%的甲溶液稀释成10%的甲溶液。
(3)要从甲的饱和溶液中获得甲的晶体,最好采用______的方法。
(4)如图2所示,20℃时,把试管放入盛有乙的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则使烧杯中的物质出现该现象的组合可能为______(填序号)。
①水和氢氧化钠固体 ②水和浓硫酸 ③水和氢氧化钙固体
【答案】 t1 不能 降温(或降温结晶) ①②
【解析】本题考查了溶解度曲线的应用和物质溶解时能量的变化。
(1)根据溶解度曲线。在温度为t1℃时,甲、乙两种物质的溶解度相等;
(2)t2℃时,甲的溶解度是60g,即t2℃时,100g的水中最多溶解60g的甲,t2℃时甲的饱和溶液的溶质质量分数=![]() ×100%=37.5%,t2℃时,不能配成60%的甲溶液。t2℃时,不能用60%的甲溶液稀释成10%的甲溶液;
×100%=37.5%,t2℃时,不能配成60%的甲溶液。t2℃时,不能用60%的甲溶液稀释成10%的甲溶液;
(3)甲的溶解度受温度影响较大。要从甲的饱和溶液中获得甲的晶体,最好采用降温(或降温结晶)的方法;
(4)镁与盐酸反应放热,C的溶解度随温度的升高而减少,烧杯中出现浑浊。氢氧化钠固体溶于水放热,浓硫酸溶于水放热,氢氧化钙固体溶于水,温度基本不变。烧杯中的物质出现该现象的组合可能为①②。

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目