题目内容
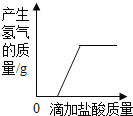
【题目】某实验员老师在处理实验室废液时,发现有一瓶含氢氧化钠和碳酸钠的溶液100g,为了处理废液,他向溶液中加入稀盐酸至刚好没有气泡产生为止,共用去14.6%的稀盐酸100g,最终得到溶液195.6g,用 pH 试纸定为中性后才倒入下水道。则此溶液中钠元素的质量分数为( )
A.4.6%B.5.3%C.9.2%D.11.7%
【答案】C
【解析】
向废液中加入稀盐酸,稀盐酸先和氢氧化钠反应生成氯化钠和水,再和碳酸钠反应生成氯化钠、二氧化碳和水,化学方程式为:![]() ,
,![]() ,根据方程式可知,最终钠元素都是以氯化钠的形式存在,故氯离子和钠离子的个数比为1:1。因为用去14.6%的稀盐酸100g,氯元素的质量为
,根据方程式可知,最终钠元素都是以氯化钠的形式存在,故氯离子和钠离子的个数比为1:1。因为用去14.6%的稀盐酸100g,氯元素的质量为![]() ,则钠元素的质量为
,则钠元素的质量为 ![]() ,因为钠元素在反应前后质量不变,故此溶液中钠元素的质量分数为
,因为钠元素在反应前后质量不变,故此溶液中钠元素的质量分数为![]() ,故选C。
,故选C。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】为探究盐酸的化学性质,某化学小组做了如下实验:
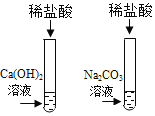
将反应后两只试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
[提出问题]滤液中溶质的成分是什么?
[假设与猜想]猜想一: NaCl
猜想二: NaCl 和CaCl2
猜想三: NaCl、Ca(OH)2 和HCl
猜想四:___________。
[讨论与交流]经讨论同学们一致认为猜想_________是错误的。原因是____________(用化学方程式解释)
[实验与结论]
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量碳酸钠溶液 | 无现象 | 猜想四成立 |
取少量滤液于试管中,滴加适量_______________ | ______________________ |
[拓展与迁移]稀盐酸和稀硫酸有相似的化学性质,是因为它们的溶液中都存在_______________。