题目内容
【题目】叠氮化钠![]() 被广泛应用于汽车安全气囊,汽车经撞击后,30毫秒内引发
被广泛应用于汽车安全气囊,汽车经撞击后,30毫秒内引发![]() 迅速完全分解生成两种单质。
迅速完全分解生成两种单质。
![]() 若因为撞击在气囊内产生
若因为撞击在气囊内产生![]() 的质量为21g,则分解的叠氮化钠质量为______g。
的质量为21g,则分解的叠氮化钠质量为______g。
![]() ______
______![]() 填化学式
填化学式![]() 。
。
![]() 已知
已知![]() ,根据
,根据![]() 中的化学方程式,
中的化学方程式,![]() 与足量的反应物完全反应能得到______
与足量的反应物完全反应能得到______![]() 。
。
【答案】![]() CuO 135
CuO 135
【解析】
(1)叠氮化钠NaN3被广泛应用于汽车安全气囊,汽车经撞击后,30毫秒内引发叠氮化钠迅速完全分解生成两种单质,即氮气和钠,对应的化学方程式2NaN3![]() 2 Na+3N2↑,
2 Na+3N2↑,
解:设生成21g氮气消耗的叠氮化钠的质量为X,
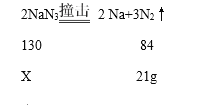
![]() =
=![]() 解得X=32.5g,故填32.5g;
解得X=32.5g,故填32.5g;
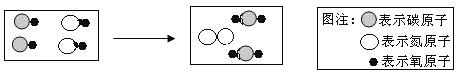
(2)根据质量守恒定律,反应前后钠和氮原子的种类和数目都不变,反应前还差1个铜原子和1个氧原子,结合给出的关系可知反应的化学方程式为2NaN3+ CuO= Na2O+3N2↑+Cu,故填CuO;
(3)设130g叠氮化钠与足量的反应物完全反应能得到的CuCl2的质量为y,根据化学方程式2NaN3+ CuO= Na2O+3N2↑+Cu和反应Cu+Cl2![]() CuCl2可得出叠氮化钠和氯化铜的关系,
CuCl2可得出叠氮化钠和氯化铜的关系,
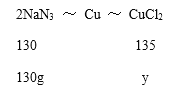
![]() =
=![]() 解得y=135g,故填135。
解得y=135g,故填135。

 阅读快车系列答案
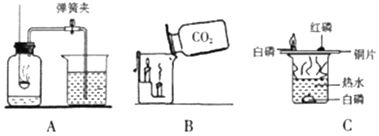
阅读快车系列答案【题目】(1)不同实验对反应速率有不同要求。某同学探究CO2制取实验,按要求答题。
限选控制反应速率的方法:①反应物的浓度 ②反应物的状态
限选试剂:A.稀盐酸 B.浓盐酸 C.块状石灰石 D.碳酸钠溶液 E.粉末状石灰石
填写下表并回答相关问题。
实验名称 | 控制速率的方法 | 所选用的最佳试剂 |
灭火器反应原理 | ① | ______和D |
CO2的实验室制法 | _____________ | A和C |
写出灭火器反应原理的化学方程式______________。
(2)已知:CO2和SO2既有相似性,又有差异性。
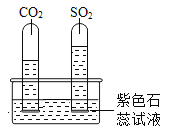
实验一:水槽中滴入紫色石蕊,将收集满两种气体的试管同时倒立于其中,片刻后实验现象如右图所示,说明相同条件下的溶解性:SO2_____ (填“>”或“<”)CO2,试管内溶液变成______色。
实验二:已知镁条在CO2中剧烈燃烧的化学方程式为:2Mg+CO2![]() 2MgO+C,试推测镁条在SO2中燃烧的现象为:剧烈燃烧,_______________________________。
2MgO+C,试推测镁条在SO2中燃烧的现象为:剧烈燃烧,_______________________________。