题目内容
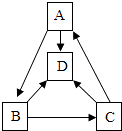
【题目】如图是探究燃烧条件的实验装置,有关该实验的说法不正确的是( ) 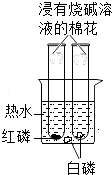
A.只有左侧试管中的红磷能燃烧
B.只有右侧试管中的白磷能燃烧
C.磷燃烧的反应属于氧化反应
D.烧碱溶液的作用是吸收燃烧产物,减轻污染
【答案】A
【解析】解:A.红磷的着火点是200℃左右,热水的温度达不到其着火点,所以红磷不能燃烧,故错误; B.白磷的着火点较低,热水的温度达到了白磷的着火点,且与氧气接触,所以白磷发生了燃烧,故正确;
C.磷燃烧是磷与氧气发生的化学反应,属于氧化反应,故正确;
D.白磷燃烧生成的五氧化二磷是一种有毒物质,可以与氢氧化钠反应,所以烧碱溶液的作用是吸收燃烧产物,减轻空气污染,故正确.
故选A.
根据燃烧的条件进行分析,物质具有可燃性,可燃物与氧气接触,温度达到可燃物的着火点,磷燃烧能生成五氧化二磷,五氧化二磷散逸到空气中易造成污染.

 阅读快车系列答案
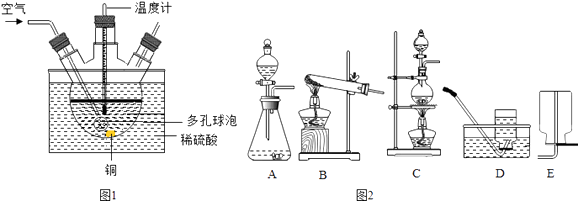
阅读快车系列答案【题目】实验室部分装置如图所示,请回答下列问题. 
(1)请选择制取氧气的发生装置和收集装置,填写在如表中(填字母).
选用药品 | 发生装置 | 收集装置 |
H2O2溶液、MnO2 | ||
KMnO4 |
(2)实验室用高锰酸钾制取氧气的文字表达式是 .
(3)如果用F装置收集氧气,导管口开始有气泡放出时,不宜立即收集的原因是 , 当气泡地放出时,再收集,验满的方法是 .
(4)实验室用过氧化氢制取氧气的文字表达式是 ,
(5)使用装置B的优点是(答一点).
【题目】莫凡同学完成镁与稀盐酸反应的实验室,观察到有灰白色沉淀生成的“异常”现象,引起了他的兴趣,并进行了以下探究.
(1)【初步探究】出现灰白色沉淀是否为偶然现象. 【实验Ⅰ】向4份相同体积与浓度的稀盐酸中分别加入一定长度的某种镁带,现象如下:
实验组别 | A | B | C | D |
镁带长度 | 1cm | 2cm | 3cm | 4cm |
沉淀量 | 无沉淀生成 | 少量沉淀 | 沉淀较多 | 沉淀很多 |
【实验结论】并非偶然,据表分析,是实验出现“异常”的主要因素.
【再次探究】该沉淀的成分
【猜想假设】猜想1:Mg;猜想2:MgCl2
【实验Ⅱ】
序号 | 实验操作 | 实验现象 | 实验结论 |
① | 取1g样品,加入足量 | 未见气泡 | 猜想1错误 |
② | 取1g样品,加入5mL蒸馏水,振荡 | 沉淀未溶解 | 猜想2错误 |
③ | 取1g MgCl2固体,加5mL蒸馏水,振荡 | 固体全部溶解 |
(2)【交流讨论】 ①莫凡同学做出猜想Ⅰ的依据是他认为反应物Mg过量,作出猜想2的依据是他认为生成物MgCl2 .
②从实验设计的角度讲,实验③的作用是 .
(3)【深入探究】该沉淀的物质组成 【查阅资料】
灰白色沉淀的成分为碱式氯化镁,它存在多种组成,化学式可表示为Mgx(OH)yClznH2O[即每份Mgx(OH)yClz结合了n份H2O],它受热分解可产生氧化镁、氯化氢和水.
【实验Ⅲ】
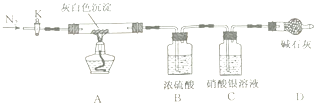
洗去沉淀表面杂质并室温晾干,取其7.07g,用如图装置(夹持仪器未画出)按照正确的操作步骤进行实验,待反应停止后,测得硬质玻璃管中剩余固体质量为4.00g,装置B的质量增加了2.34g.
【问题讨论】
①反应停止后,应继续通入N2一段时间,目的是 .
②该沉淀中,镁、氯的离子个数比n(Mg2+):n(Cl﹣)= .
③若沉淀Mgx(OH)yClznH2O中,n=5,则X、Y、Z的数值依次为 .