题目内容
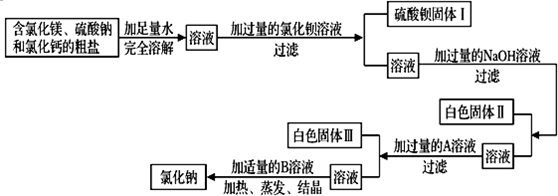
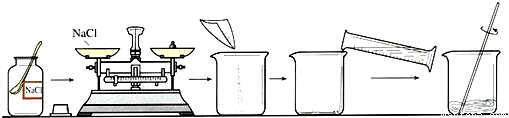
海洋是丰富的化学资源宝库.通过晾晒海水可以得到含有较多杂质(杂质包含CaCl2和MgSO4和泥沙等)的粗盐.(1)在做粗盐初步提纯的实验时,要进行如图所示的实验操作.
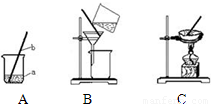
①操作C中看到 时,停止加热.
②经过以下三步操作后能否得到纯净的食盐 (填“能”或“否”)
(2)某粗盐样品20克(含有可溶性的氯化钙杂质和不溶性的泥沙其他杂质忽略不计)分成二等份.
①常温下,将一份该粗盐样品完全溶解于一定量水中,过滤得到1.5克泥沙.
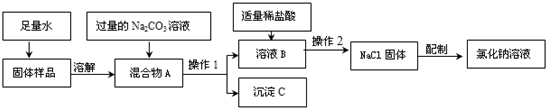
②学校化学兴趣小组将另一份粗盐样品来配制一定质量分数的NaCl溶液,实验的流程如图:(假设每一份样品中泥沙均匀等量的分布)
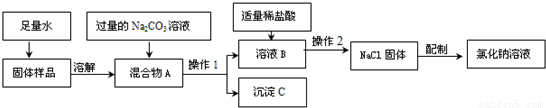
请回答:
(a) 写出过量碳酸钠溶液加入到溶液A中所发生反应的化学方程式为 .
(b) 操作1的名称是 ,在溶液B中加入适量稀盐酸的目的是 .
(c)如果将沉淀C充分洗涤干燥后称量其质量为2克,试计算粗盐样品中含氯化钙质量分数?(写出计算过程)
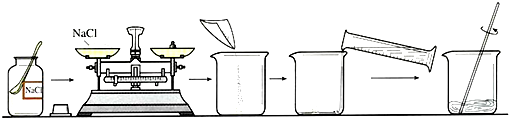
(d)若要配制50g质量分数为5%的氯化钠溶液,常按以下操作顺序进行.
请回答下列问题:计算配制50g溶质质量分数为5%的氯化钠溶液所需:
①氯化钠 g,水 g.
②用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 .
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节平衡 D.移动游码.
【答案】分析:(1)①根据蒸发时的操作要领分析判断;
②根据过滤能去除的杂质成分分析即可;
(2)(a)依据碳酸钠和氯化钙反应的情况书写方程式即可;(b)从操作1分离混合物的情况分析判断(c)从沉淀的量利用化学方程式求出氯化钙的质量,然后进行相关的计算即可;
(d)从配制一定溶质质量分数的实验步骤分析解决;
解答:解:(1)①蒸发时为防止固体飞溅,所以当溶液中出现多量固体时即停止加热.
②过滤能去除的杂质是不溶性杂质,不能除掉可溶性杂质,所以此时得到的实验不纯净;
(2)(a)碳酸钠和氯化钙反应会生成碳酸钙和氯化钠,其方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl;
(b)从操作1分离混合物是固体和液体可知,该处的操作是过滤;
(c)设食盐中氯化钙的质量是x
Na2CO3+CaCl2=CaCO3↓+2NaCl
111 100
x 2g
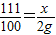
x=2.22g
该食盐中氯化钙的质量分数=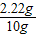 ×100%=22.2%
×100%=22.2%
(d)①配制50g溶质质量分数为5%的氯化钠溶液所需的氯化钠为50g×5%=2.5g,水的质量是50g-2.5g=47.5g;
②托盘天平的指针偏向左盘,说明左盘重,由于这是定量测量因此应减少适量氯化钠固体;
故答案为:(1)①溶液中有多量固体出现;
②否;
(2)(a)Na2CO3+CaCl2=CaCO3↓+2NaCl;
(b)从操作1分离混合物是固体和液体可知,该处的操作是过滤;
(c)设食盐中氯化钙的质量是x
Na2CO3+CaCl2=CaCO3↓+2NaCl
111 100
x 2g
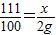
x=2.22g
该食盐中氯化钙的质量分数=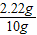 ×100%=22.2%.
×100%=22.2%.
答:食盐中氯化钙的质量分数是22.2%.
(d)①2.5g;47.5g;
②B
点评:注意混合物的分离方法,探究实验操作的注意事项,熟练常用仪器的名称和选用,加强溶质质量分数的简单计算是解题的关键.
②根据过滤能去除的杂质成分分析即可;
(2)(a)依据碳酸钠和氯化钙反应的情况书写方程式即可;(b)从操作1分离混合物的情况分析判断(c)从沉淀的量利用化学方程式求出氯化钙的质量,然后进行相关的计算即可;
(d)从配制一定溶质质量分数的实验步骤分析解决;
解答:解:(1)①蒸发时为防止固体飞溅,所以当溶液中出现多量固体时即停止加热.
②过滤能去除的杂质是不溶性杂质,不能除掉可溶性杂质,所以此时得到的实验不纯净;
(2)(a)碳酸钠和氯化钙反应会生成碳酸钙和氯化钠,其方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl;
(b)从操作1分离混合物是固体和液体可知,该处的操作是过滤;
(c)设食盐中氯化钙的质量是x
Na2CO3+CaCl2=CaCO3↓+2NaCl
111 100
x 2g
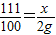
x=2.22g
该食盐中氯化钙的质量分数=
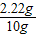 ×100%=22.2%
×100%=22.2%(d)①配制50g溶质质量分数为5%的氯化钠溶液所需的氯化钠为50g×5%=2.5g,水的质量是50g-2.5g=47.5g;
②托盘天平的指针偏向左盘,说明左盘重,由于这是定量测量因此应减少适量氯化钠固体;
故答案为:(1)①溶液中有多量固体出现;
②否;
(2)(a)Na2CO3+CaCl2=CaCO3↓+2NaCl;
(b)从操作1分离混合物是固体和液体可知,该处的操作是过滤;
(c)设食盐中氯化钙的质量是x
Na2CO3+CaCl2=CaCO3↓+2NaCl
111 100
x 2g
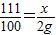
x=2.22g
该食盐中氯化钙的质量分数=
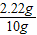 ×100%=22.2%.
×100%=22.2%.答:食盐中氯化钙的质量分数是22.2%.
(d)①2.5g;47.5g;
②B
点评:注意混合物的分离方法,探究实验操作的注意事项,熟练常用仪器的名称和选用,加强溶质质量分数的简单计算是解题的关键.

练习册系列答案
相关题目


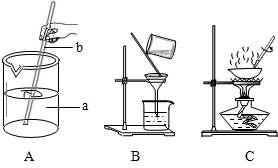 (1)海洋是丰富的化学资源宝库.通过晾晒海水,可以得到含少量泥沙的粗盐.在做粗盐初步提纯的实验时,要进行如下图所示的实验操作.
(1)海洋是丰富的化学资源宝库.通过晾晒海水,可以得到含少量泥沙的粗盐.在做粗盐初步提纯的实验时,要进行如下图所示的实验操作.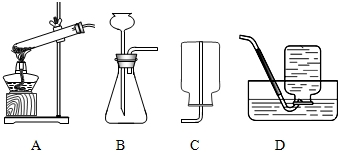
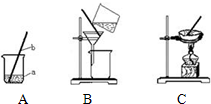 (1)在做粗盐初步提纯的实验时,要进行如图所示的实验操作.
(1)在做粗盐初步提纯的实验时,要进行如图所示的实验操作.