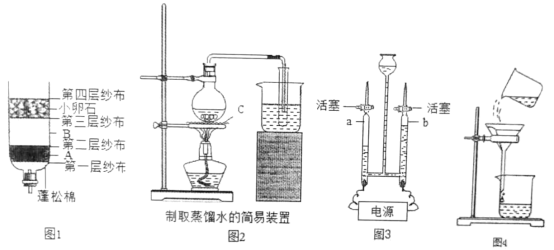
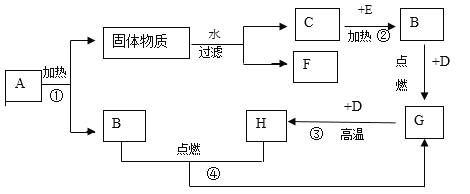
题目内容
【题目】硫酸是实验室最常用的药品之一。
(1)稀释浓硫酸:稀释时一定要将浓硫酸沿容器壁慢慢注入盛水的烧杯里并不断搅拌。此时若用手接触烧杯外壁,有_____的感觉,搅拌时常用的仪器是_____,稀释时如果将水注入浓硫酸中产生的后果是_____,写出稀硫酸中阴离子的离子符号_____。
(2)100g某硫酸恰好与13g锌完全起反应。试计算这种硫酸中溶质的质量分数_____。
【答案】发烫或发热 玻璃棒 水沸腾硫酸液滴向四周飞溅 SO42- 19.6%
【解析】
(1)浓硫酸溶于水时,放出大量的热。稀释浓硫酸:稀释时一定要将浓硫酸沿容器壁慢慢注入盛水的烧杯里并不断搅拌。此时若用手接触烧杯外壁,有发烫或发热的感觉,搅拌时常用的仪器是玻璃棒,稀释时如果将水注入浓硫酸中产生的后果是水沸腾硫酸液滴向四周飞溅,稀硫酸中阴离子是硫酸根离子,其离子符号为:SO42-;
(2)设:这种硫酸中溶质的质量分数为x。
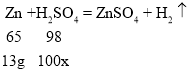
![]() x=19.6% 。
x=19.6% 。

练习册系列答案
相关题目