题目内容
【题目】将100g含有少量碳酸钾的氯化钾样品加入50g盐酸中完全反应且溶解,气体全部逸出,得到145.6g溶液.则:
(1)产生的气体质量为________g.
(2)样品中氯化钾的质量分数_______;
(3)所得溶液中溶质质量分数_______(计算结果精确到0.1%).
【答案】4.4 86.2% 69.4%
【解析】
(1)根据质量守恒定律可得,生成的二氧化碳的质量=100g+50g-145.6g=4.4g;
(2)设样品中碳酸钾的质量为x,生成的氯化钾的质量为y。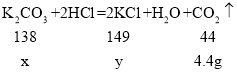
![]()
![]()
x=13.8g y=14.9g
则样品中氯化钾的质量分数为![]()
所得溶液中氯化钾的质量分数为![]()
答:(1)产生的气体质量为 4.4g;
(2)样品中氯化钾的质量分数为86.2%;
(3)所得溶液中氯化钾的质量分数约为69.4%。

练习册系列答案
相关题目
【题目】目前使用的燃料大多来自化石燃料。
(1)写出天然气中甲烷完全燃烧的化学方程式______。
(2)分析下表,与煤相比,用天然气作燃料的优点有______。
1g物质完全燃烧 | ||
产生二氧化碳的质量/g | 放出的热量/kJ | |
甲烷 | 2.75 | 56 |
煤碳 | 3.67 | 32 |
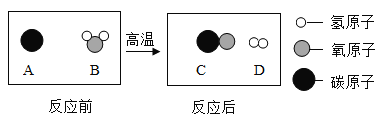
(3)为提高煤的利用率,可将其转化为可燃性气体,该反应的微观示意图如下,则生成物的分子个数比为_____。