题目内容
【题目】酸和碱能发生中和反应,它在日常生活和工农业生产中有着广泛的应用,如图表示盐酸和氢氧化钠溶液发生反应时烧杯中溶液的pH随加入液体体积的变化曲线及相关的实验操作,请从中获取信息,回答下列问题
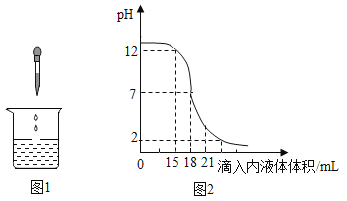
(1)①烧杯中盛放的是_____溶液。
②曲线上坐标为(18,7)的点所表示的意义_____。
③曲线上坐标为(15,12)的点表示的溶液中的微粒有_____(用化学用语表示)。
(2)小明完成上述实验几天后发现,忘记盖上盛放氢氧化钠溶液试剂瓶的瓶塞,请帮助小明完成如下实验方案来检验氢氧化钠溶液是否变质。
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取少量溶液于试管中,滴加几滴稀盐酸 | 没有气体产生 | 没有变质 |
方案二 | 取少量溶液于试管中,滴加几滴氯化钡溶液 | 已经变质 |
①你认为方案一的实验设计是否正确?_____(填“是”或“否”)
②请写出方案二中的实验现象_____
③请写出方案二中发生反应的化学方程式_____。
④若该氢氧化钠溶液部分变质,则下列实验现象及结论合理的是_____
A 取一定量溶液样品,滴入稀盐酸,立即有大量气体产生
B 取一定量溶液样品,滴入适量的澄清石灰水,过滤,向滤液中滴加酚酞溶液,溶液变红,证明原样品中含有氢氧化钠
C 取一定量溶液样品,滴入足量的氯化钙溶液,过滤,向滤液中滴加酚酞溶液,溶液变红,证明原样品中含有氢氧化钠
D 向溶液样品中加入过量的澄清石灰水充分反应,过滤,可除去样品中的杂质
【答案】氢氧化钠 在加入稀盐酸18mL时,稀盐酸与氢氧化钠恰好反应,溶液的pH是7 Na+、Cl-、OH-、H2O 否 产生白色沉淀 BaCl2+Na2CO3=BaCO3↓+2NaCl C
【解析】
(1)①由图象可知,开始时溶液的pH大于7,说明了烧杯中盛放的是氢氧化钠溶液。
②由图示可知,曲线上坐标为(18,7)的点所表示的意义是:在加入稀盐酸18mL时,稀盐酸与氢氧化钠恰好反应,溶液的pH是7。
③曲线上坐标为(15,12)的点表示在加入稀盐酸15mL时,稀盐酸未将氢氧化钠完全反应,溶液中有生成的氯化钠和未反应的氢氧化钠,微粒有:Na+、Cl-、OH-、H2O。
(2)①方案一的实验设计不正确,理由是:在氢氧化钠和碳酸钠的混合液中,滴入少量稀盐酸时,稀盐酸先与氢氧化钠反应。
②氢氧化钠和二氧化碳反应生成碳酸钠变质,由于碳酸钠能与氯化钡反应生成了碳酸钡沉淀和氯化钠,所以反应的现象是:产生了白色沉淀;
③由上述分析可知,方案二中发生反应的化学方程式是:BaCl2+Na2CO3=BaCO3↓+2NaCl。
④A、由于部分变质的氢氧化钠一定含有碳酸钠,滴入稀盐酸,应该是先没有气泡产生(此时和氢氧化钠反应),等到氢氧化钠反应完毕,才和碳酸钠反应,此时才会有气体产生,故选项错误;
B、由于滴入适量的澄清石灰水与碳酸钠反应也会生成碱氢氧化钠,所以滴加酚酞溶液,溶液变红,不能证明原样品中含有氢氧化钠,故选项错误;
C、由于部分变质的氢氧化钠一定含有碳酸钠,所以加入中性氯化钡溶液,会生成碳酸钡白色沉淀和中性氯化钠,所以滴加酚酞溶液,溶液变红,能证明原样品中含有氢氧化钠,故选项正确;
D、向溶液样品中加入适量的澄清石灰水至恰好完全反应,生成了氢氧化钠和碳酸钙白色沉淀,沉淀过滤,可除去样品中的杂质,但澄清的石灰水过量,所以又引入氢氧化钙杂质,故选项错误。故选C。

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案