题目内容
【题目】如图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题:
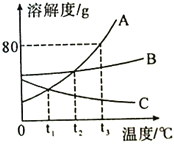
(1)t2℃时,A、B、C三种物质的溶解度大小关系是 .
(2)t3℃时,将30gA物质加入到50g水中,充分溶解后,所得溶液是 (填“饱和”或“不饱和”)溶液.所得溶液溶质质量分数为
(3)室温下,将盛有A的饱和溶液的试管放入盛水的烧杯中,再向烧杯内的水中加入一定量的并NH4NO3并搅拌,试管内可以观察到的现象是 .
(4)将t2℃时A、B、C三种饱和溶液同时降温至t1℃时,所得溶液中溶质的质量分数的大小关系是 .
【答案】(1)A=B>C;
(2)不饱和,37.5%;
(3)有晶体析出;
(4)B>A>C.
【解析】
试题分析:根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解:(1)通过分析溶解度曲线可知,t2℃时,A、B、C三种物质的溶解度大小关系是A=B>C;
(2)t3℃时,A物质的溶解度是80g,所以将30gA物质加入到50g水中,充分溶解后,所得溶液是不饱和溶液,所得溶液溶质质量分数为![]() ×100%=37.5%;
×100%=37.5%;
(3)A物质的溶解度随温度的降低而减小,硝酸铵溶于水,溶液温度降低,所以室温下,将盛有A的饱和溶液的试管放入盛水的烧杯中,再向烧杯内的水中加入一定量的并NH4NO3并搅拌,试管内可以观察到的现象是有晶体析出;
(4)t1℃时,B物质的溶解度最大,A物质次之,A、B物质的溶解度随温度的降低而减小,会析出晶体,C物质的降低温度,不会析出晶体,应该按照t2℃时进行计算,所以将t2℃时,A、B、C三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是B>A>C.
故答案为:(1)A=B>C;
(2)不饱和,37.5%;
(3)有晶体析出;
(4)B>A>C.

【题目】
元素名称 | 钠 | 钙 | 铝 | 氢 | 氯 | 氧 | 硫 |
(1)如表元素中,在地壳内含量最多的金属元素符号是 ;在人体内含量最多的元素符号是 ;水中含有+1价的元素符号是 .
(2)氯化钙的化学式 ;Na2SO3中S元素的化合价为 .
(3)水是生命的源泉,也是不可缺少的资源.
①下列物质中属于纯净物的是(填字母) .
A.汽水 B.蒸馏水 C.矿泉水 D.冰水
②如图为活性炭净水器示意图.活性炭的作用是 .
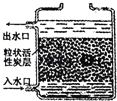
③自来水厂净水过程中需加消毒剂.二氧化氯(ClO2)是新一代饮用水的消毒剂,其中氯元素的化合价为 .
【题目】下列化学方程式与对应反应类型均正确的是( )
化学方程式 | 反应类型 | |
A | H2O | 分解反应 |
B | CaO+H2O═Ca(OH)2 | 化合反应 |
C | 2Fe+6HCl═2FeCl3+3H2↑ | 置换反应 |
D | SO3+2NaOH═Na2SO4+H2O | 复分解反应 |
A.A B.B C.C D.D
【题目】根据如表回答问题.
温度(℃) | 20 | 40 | 50 | 60 | 80 | |
溶解度 (g/100g水) | NaCl | 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
NH4Cl | 37.2 | 45.8 | 50.4 | 55.2 | 65.6 | |
KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 | |
①20℃时,溶解度最大的物质是
②50℃时,100g水中最多溶解NaCl g
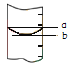
③量筒的局部示意见图,量取水时应沿 视线(选填“a”或“b”)进行读数, 视线(选填“a”或“b”)对应的读数较大.
④A是80℃含有120g水的KNO3溶液,经过如下操作,得到102gKNO3固体.
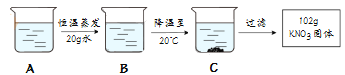
I.A溶液为 (选填“饱和”或“不饱和”)溶液
II.对以上过程的分析,正确的是 (选填编号)
a.A到B的过程中,溶质质量没有改变
b.B中溶质与溶剂的质量比为169:100
c.开始析出KNO3固体的温度在60℃至80℃之间
d.A溶液的质量等于222g.