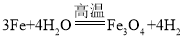题目内容
【题目】“质量守恒定律”是我们学习化学的一个重要定律。某兴趣小组同学想通过实验验证质量守恒定律,请你参与他们的探究吧。
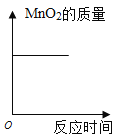
[查阅资料]①![]() ②
②![]()
[提出问题]设计实验验证质量守恒定律。
[进行实验]
实验一 | 实验二 | |
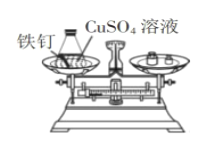
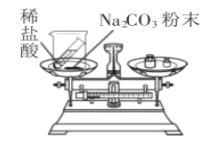
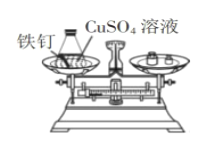
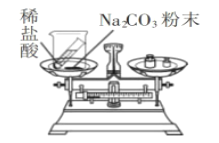
实验方案. |
|
|
实验现象 | _____。 | 有气泡冒出,天平指针向右偏转。 |
实验结论 | 反应前后质量相等。 反应的化学方程式为_____。 | 反应前后质量不相等。 |
[反思评价]通过讨论,同学们发现实验二中有气体逸出,导致指针右偏转。得到启示:在探究化学反应前后各物质质量总和是否相等时,凡有气体生成或参加的反应,一定要在_____中进行。
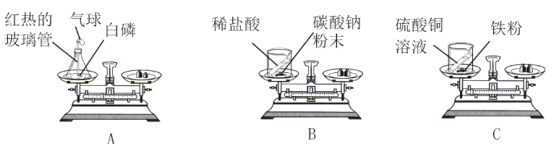
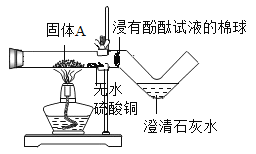
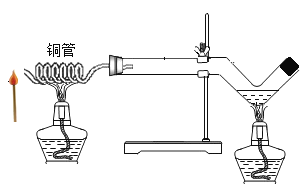
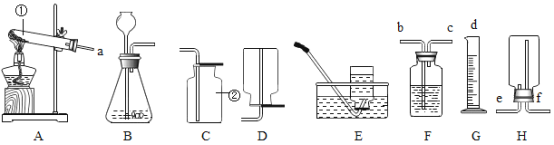
[改进装置]如图是同学们对实验二中的装置进行的如下改进,你认为最佳装置是_____(填序号),说一说另一装置的不足之处:_____。

[解释应用](1)化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
(2)铜丝在火焰上灼烧,灼烧后的“铜丝”的质量_____(填“大于”或“小于”)原来铜丝的质量,原因是_____。
【答案】铁钉表面有红色物质析出,溶液由蓝色变为浅绿色;天平指针没有偏转 ![]() 密闭容器 B A装置中反应产生气体,气球膨胀,浮力增大,导致称量结果不准确 大于 灼烧铜丝,铜丝会和氧气反应生成氧化铜,所以灼烧后的质量大于灼烧前的质量
密闭容器 B A装置中反应产生气体,气球膨胀,浮力增大,导致称量结果不准确 大于 灼烧铜丝,铜丝会和氧气反应生成氧化铜,所以灼烧后的质量大于灼烧前的质量
【解析】
铁和硫酸铜反应生成铜和硫酸亚铁,稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,铜丝和氧气加热生成氧化铜。
[进行实验]铁和硫酸铜反应生成铜和硫酸亚铁,稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳。
实验一 | 实验二 | |
实验方案. |
|
|
实验现象 | 铁钉表面有红色物质析出,溶液由蓝色变为浅绿色;天平指针没有偏转。 | 有气泡冒出,天平指针向右偏转。 |
实验结论 | 反应前后质量相等。 反应的化学方程式为 | 反应前后质量不相等。 |
[反思评价]在探究化学反应前后各物质质量总和是否相等时,凡有气体生成或参加的反应,一定要在密闭容器中进行。
[改进装置]最佳装置是B,A装置的不足之处是反应产生气体,气球膨胀,浮力增大,导致称量结果不准确。
[解释应用] (2)铜丝在火焰上灼烧,灼烧后的“铜丝”的质量大于原来铜丝的质量,原因是灼烧铜丝,铜丝会和氧气反应生成氧化铜,所以灼烧后的质量大于灼烧前的质量。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案