题目内容
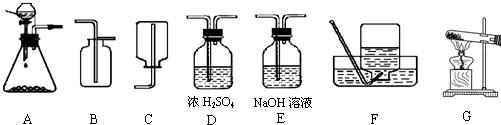
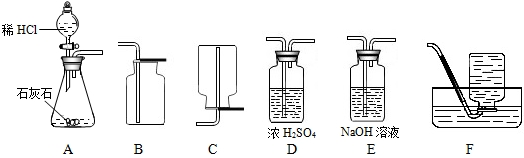
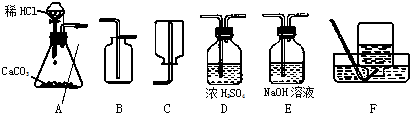
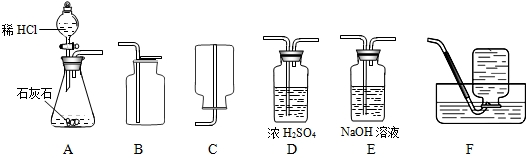
18、为了研究CO2的性质,需要制取并收集CO2气体.以下是老师提供的一些实验装置.
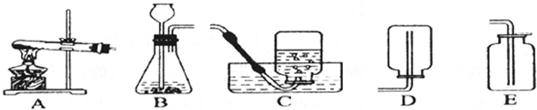
(1)制取并收集CO2气体,可采用的装置组合是
(2)实验室制取CO2的化学方程式
(3)实验室用过氧化氢制取并收集氧气,可采用的装置组合是

(1)制取并收集CO2气体,可采用的装置组合是
B、E
(填字母,下同),检验集气瓶中CO2是否收集满的方法是将燃着的木条放在集气瓶口,若木条熄灭,证明已经收集满
,若在该实验中气体无法收集满,可能的原因是导管未深入到集气瓶的底部
.(2)实验室制取CO2的化学方程式
CaCO3+2HCl=CaCl2+H2O+CO2↑
.(3)实验室用过氧化氢制取并收集氧气,可采用的装置组合是
B、C或B、E
.分析:此题是一道综合性较强的题型,涉及了实验室制取气体的发生装置和收集装置的选取,二氧化碳收满的验证,化学方程式的书写等等.
解答:解:(1)由于实验室制取二氧化碳用稀盐酸和大理石或石灰石反应,所得CO2气流平稳且不需要加热,气体又较为纯净,所以选用稀盐酸制CO2最合适.所以发生装置选B.
收集装置选E,用向上排空气法收集二氧化碳(因为二氧化碳密度比空气大).不能用排水法收集二氧化碳(因为二氧化碳溶于水).根据二氧化碳不燃烧也不支持燃烧的性质,可以用带火星的木条检验是否收满.如果用排空气法收二氧化碳时,应该把导管伸到集气瓶底,便于排尽空气.
(2)反应的方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑,注意条件和配平.
(3)实验室制取并收集氧气,若用用过氧化氢制取,则过氧化氢制取氧气时,不需要加热,所以发生装置选B,收集装置可以选C或E均可.
故答案为:(1)B、E、将燃着的木条放在集气瓶口,若木条熄灭,证明已经收集满;导管未深入到集气瓶的底部.
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)B;C或B、E
收集装置选E,用向上排空气法收集二氧化碳(因为二氧化碳密度比空气大).不能用排水法收集二氧化碳(因为二氧化碳溶于水).根据二氧化碳不燃烧也不支持燃烧的性质,可以用带火星的木条检验是否收满.如果用排空气法收二氧化碳时,应该把导管伸到集气瓶底,便于排尽空气.
(2)反应的方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑,注意条件和配平.
(3)实验室制取并收集氧气,若用用过氧化氢制取,则过氧化氢制取氧气时,不需要加热,所以发生装置选B,收集装置可以选C或E均可.
故答案为:(1)B、E、将燃着的木条放在集气瓶口,若木条熄灭,证明已经收集满;导管未深入到集气瓶的底部.
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)B;C或B、E
点评:做此类题时,应根据反应物的状态及反应条件进行灵活选择制取和收集装置,正确书写方程式.注意知识间的相同和区别.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目