题目内容
【题目】将30g碳酸钠溶液与48.2g氯化钡溶液混合,碳酸钠和氯化钡两种物质恰好完全反应。过滤,所得滤液质量为58.5g,试计算:(反应的化学方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl)
⑴反应后生成的沉淀质量为___g。
⑵所得滤液中溶质的质量分数为多少_______?
【答案】19.720%.
【解析】
(1)根据质量守恒定律可知:反应后溶液质量的减少量就是生成的沉淀的质量;
(2)根据沉淀的质量结合方程式算出氯化钠的质量,并据溶质的质量分数计算公式化进行解答。
(1)反应后生成沉淀的质量是:30g+48.2g﹣58.5g=19.7g;
(2)设溶液中溶质NaCl的质量为x
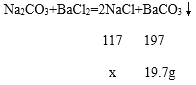
![]() x=11.7g
x=11.7g
所得滤液中溶质的质量分数为:![]() =20%。
=20%。
答:反应后生成的沉淀质量为19.7g;
(2)所得滤液中溶质的质量分数为20%。

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目