题目内容
【题目】某校兴趣小组的同学从水泥厂拿来一块石灰石样品,技术员告诉他们此样品中含有的杂质难溶于水,不能与盐酸反应。为了测定该样品的纯度,同学取用8.00g这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸100克分5次加入,充分反应后,经过滤、干燥等操作后称量,得到如下数据:
实 验 次 数 | 1 | 2 | 3 | 4 | 5 |
加入稀盐酸的质量/g | 20.0 | 20.0 | 20.0 | 20.0 | 20.0 |
剩余固体的质量/g | 6.00 | m | 2.00 | 1.20 | 1.20 |
试回答下列问题:
(l)表中m的值为_____________。
(2)该石灰石样品的纯度是__________。
(3)反应生成的气体质量是多少克?______________
(4)试计算稀盐酸的质量分数 ____________。
【答案】4 85% 2.992 7.3%
【解析】
本题考查了与实验相关的化学方程式计算。首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等,然后根据所给的问题情景细致地分析题意,并细心地探究、推理后,按照题目要求进行解答。
(l)根据表格数据可得,每消耗20g盐酸,固体质量减少2.00g,所以m的值为6.00﹣2.00g=4.00g,由表中数据可知第四次和第五次固体的质量不再变化,所以杂质的质量为1.20g;
(2)石灰石的质量分数为:![]() ×100%=85.0%;
×100%=85.0%;
(3)设:生成二氧化碳的质量为x。
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
6.8g x
![]() =
=![]() x=2.992g
x=2.992g
设:与2.00g石灰石完全反应消耗 HCl的质量为y。
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
4.00g y
![]() =
=![]() y=1.46g
y=1.46g
稀盐酸的质量分数=![]() ×100%=7.3%
×100%=7.3%

 名校课堂系列答案
名校课堂系列答案【题目】甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:
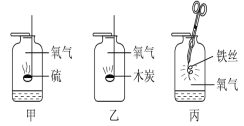
(1)所发生的三个反应有多个共同的特点,分别是:①________,②______。(写两点即可)
(2)甲、丙两实验集气瓶中均放少量水,甲中加入少量水的目的是___________,甲瓶中反应的文字表达式为__________。
(3)小明做完上述实验后,在乙中加入了一种无色液体,加该液体的目的是 _______。
(4)小明对铁丝在氧气中燃烧为什么会火星四射进行探究。他将镁条和不同含碳量的铁丝(铁丝直径均为0.4 mm)放入氧气中燃烧,并将现象记录在下表中。
物质 | 镁 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧,极少火星 | 剧烈燃烧,少量火星 | 剧烈燃烧,火星四射 |
①小明实验前将铁丝绕成螺旋状的目的是___________。
②造成铁丝在氧气中燃烧时火星四射的主要原因是 ____________。
③铁丝在氧气中燃烧的文字表达式为 ___________。