题目内容
【题目】实验室制取氧气时,某同学取一定质量的高锰酸钾加热,记录产生氧气的质量与反应时间的关系如图1所示,请回答下列问题: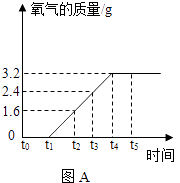
(1)请根据图中数据计算高锰酸钾的质量为多少?(写出计算过程)
(2)请在图2坐标中,画出固体中锰元素质量在t0﹣t5时段变化示意图.
(反应的化学方程式:2KMnO4 ![]() K2MnO4+MnO2+O2↑)
K2MnO4+MnO2+O2↑)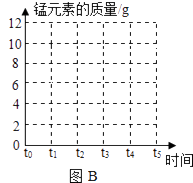
【答案】
(1)解:根据图中信息可知:t0﹣t1固体质量不变,是因为反应还未进行;t4﹣t5时固体质量不变,是因为反应进行完全;
设高锰酸钾的质量是x,由图象可知该反应生成的氧气质量是3.2g;
2KMnO4 | O2↑ |
316 | 32 |
x | 3.2g |
![]()
x=31.6g
答案:高锰酸钾的质量是31.6g
(2)解:31.6g高锰酸钾中锰元素的质量是31.6g× ![]() ×100%=11g
×100%=11g

【解析】根据化学方程式计算步骤分析,由题意可知,本题的已知条件为氧气的质量,利用氧气质量与高锰酸钾质量关系计算出高锰酸钾的质量,根据反应前后锰元素质量不变分析。
【考点精析】利用根据化学反应方程式的计算对题目进行判断即可得到答案,需要熟知各物质间质量比=系数×相对分子质量之比.

练习册系列答案
相关题目