��Ŀ����
����Ŀ���Ȼ�������Ҫ�Ļ���ԭ�ϣ�ij��ҵ̼���������������Ҫ����������һЩ������Ӧ�����������ʣ������ֹ�ҵ̼���Ϊԭ�������Ȼ��Ƶ���Ҫ������ͼ��ʾ��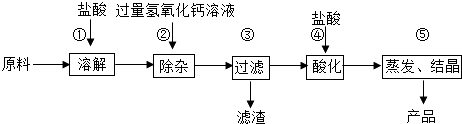
��1���ɲ���ٿ��жϹ���������ԭ���е����ʷ�Ӧ���ɵ������Ȼ������� ��
��2������۵õ�����������������������д������ڷ������ֽⷴӦ�������������Ļ�ѧ����ʽ�� ��
��3������ܼ�����������Ŀ���dz�ȥ�������������������ԣ���ȥ���������ᣮ
���𰸡�
��1��CaCl2,FeCl3
��2��3Ca��OH��2+2FeCl3=3CaCl2+2Fe��OH��3��
��3����������������,�ӷ�
���������⣺��1��̼��ƿ��Ժ����ᷴӦ�����Ȼ��ƣ������������ᷴӦ�����Ȼ��������ж�������ԭ���е����ʷ�Ӧ���ɵ������Ȼ������Ȼ��ƺ��Ȼ�������2���ڹ�ҵ̼����к��������������Լ�����������������Ժ����ᷴӦ�������Ȼ������Ȼ����ͼ�����������Ʒ�Ӧ�����������������ʿ���д���÷�Ӧ�Ļ�ѧ����ʽ��3Ca��OH��2 +2FeCl3 �T3CaCl2 +2Fe��OH��3������3�����ڼ�������������ǹ����ģ�������������Һ�к����������ƣ����ֱ���������ʹ�Ƶõ��Ȼ��Ʋ��������Լ���ϡ�������к��������ƣ���������лӷ��ԣ����Լ���ʱ����ӷ�������ʣ��Ĺ���Ϊ�Ȼ��ƣ�
���Դ��ǣ���1��CaCl2��FeCl3����2��3Ca��OH��2+2FeCl3=3CaCl2+2Fe��OH��3������3���������������ƣ��ӷ���
�����㾫�����������⣬������Ҫ�˽���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ(ע�⣺a����ƽ b������ c������)��

 ����С��ʿ���������ϵ�д�
����С��ʿ���������ϵ�д�