题目内容
【题目】结合氧气性质的有关实验,回答下列问题:
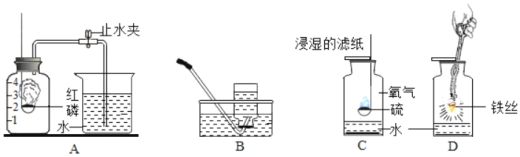
(1)用A实验验证空气中氧气的含量,能得到的正确结论是_____。
(2)用B装置收集氧气时,得到的气体不纯,造成这种后果的原因可能是_____。
(3)D实验中水的作用是_____。
(4)C实验中潮湿的滤纸和水的作用是_____。
【答案】氧气约占空气总体积的五分之一 集气瓶没有预先装满水或刚冒气泡就收集; 防止高温熔化物溅落下来炸裂瓶底; 吸收有毒气体二氧化硫,防止污染空气;
【解析】
(1)用A实验验证空气中氧气的含量,能得到的正确结论是氧气约占空气体积的![]() ,故填氧气约占空气总体积的五分之一。
,故填氧气约占空气总体积的五分之一。
(2)B实验是利用排水法收集气体,用B装置收集氧气时,得到的气体不纯,造成这种后果的原因可能是集气瓶没有预先装满水或刚冒气泡就收集,故填集气瓶没有预先装满水或刚冒气泡就收集。
(3)D组实验是铁在氧气中燃烧放出大量的热,水的作用是防止高温熔化物溅落炸裂瓶底,故填防止高温熔化物溅落下来炸裂瓶底。
(4)C实验是硫燃烧生成的二氧化硫有毒,能污染空气,二氧化硫能溶于水,水的作用是收集二氧化硫,防止污染空气,故填吸收有毒气体二氧化硫,防止污染空气。

练习册系列答案
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目