题目内容
【题目】4.6g酒精在空气中充分燃烧,生成8.8g二氧化碳和5.4g水,已知酒精的相对分子质量为46,试根据所学知识回答下列问题:
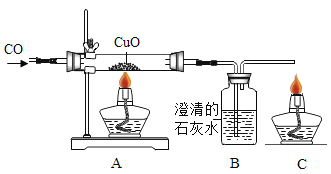
(1)设计实验证明二氧化碳和水的存在_________。
(2)运用质量守恒定律分析酒精的元素组成,并确定它的化学式_________。
【答案】点燃该物质,在火焰上方罩一干冷烧杯,烧杯内壁出现水雾,证明有水生成;迅速倒转烧杯,加入澄清石灰水,振荡,石灰水变浑浊,证明有二氧化碳生成 化学反应前后元素种类不变,生成物二氧化碳和水中有碳、氢、氧三种元素,反应物氧气中只含有氧元素。所以,该物质中一定含有碳、氢元素,可能含有氧元素。又因为化学反应前后元素的质量不变,根据8.8g二氧化碳的质量计算出碳元素质量2.4g,根据5.4g水的质量计算出氢元素质量0.6g ;碳氢元素质量之和为3g 小于4.6g,所以该物质中还含有氧元素。碳氢氧原子个数比为![]() ,又因为该物质的相对分子质量为46,而12×2+1×6+16=46,所以该物质的化学式为C2H6O
,又因为该物质的相对分子质量为46,而12×2+1×6+16=46,所以该物质的化学式为C2H6O
【解析】
生成物二氧化碳和水中有碳、氢、氧三种元素,反应物氧气中只含有氧元素。该物质中一定含有碳、氢元素,可能含有氧元素,8.8g二氧化碳和5.4g水中碳元素和氧元素的质量和为![]() ,则该物质中还含有氧元素。
,则该物质中还含有氧元素。
(1)二氧化碳能使澄清石灰水变浑浊,实验证明二氧化碳和水的存在点燃该物质,在火焰上方罩一干冷烧杯,烧杯内壁出现水雾,证明有水生成;迅速倒转烧杯,加入澄清石灰水,振荡,石灰水变浑浊,证明有二氧化碳生成。
(2)根据质量守恒定律,化学反应前后元素种类不变,生成物二氧化碳和水中有碳、氢、氧三种元素,反应物氧气中只含有氧元素。该物质中一定含有碳、氢元素,可能含有氧元素。又因为化学反应前后元素的质量不变,8.8g二氧化碳中碳元素质量为
![]() ,5.4g水中氢元素质量为
,5.4g水中氢元素质量为![]() ,8.8g二氧化碳和5.4g水中碳元素和氧元素的质量和为
,8.8g二氧化碳和5.4g水中碳元素和氧元素的质量和为![]() ,则该物质中还含有氧元素,碳氢氧原子个数比为
,则该物质中还含有氧元素,碳氢氧原子个数比为![]() ,该物质的相对分子质量为46,而
,该物质的相对分子质量为46,而
![]() ,故该物质的化学式为C2H6O。
,故该物质的化学式为C2H6O。

【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法错误的是
物质 | a | b | c | d |
反应前质量(g) | 10 | 10 | 10 | 2 |
反应后质量(g) | 待测 | 2 | 21 | 2 |
A.该反应是化合反应,d可能是催化剂
B.a、b两种物质中元素种类一定与c物质中元素种类相同
C.b物质可能是单质
D.反应后a物质的质量为3g