��Ŀ����
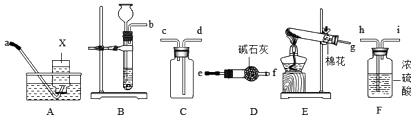
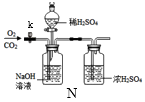
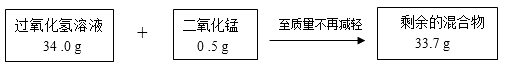
����Ŀ��ij��ȤС����ѧϰ��Ļ�ѧ����ʱ����������ͼ��ʾ��ʵ�飮 
��1���ڼ�ʵ������У�����һ֧�¶ȼ���������Һ���¶�ʱ������ϡ����IJ��ϵ��룬��Һ���¶������ߣ�����Ϊ��Һ�¶����ߵ�ԭ������д���÷�Ӧ�Ļ�ѧ����ʽ ��
��2����ʵ���еμ�����������Һ�ɹ۲쵽������������Ӧ�Ļ�ѧ����ʽ ��
��3��ʵ�������ͬѧ�ǽ��ס�������ʵ��ķ�Һ����ͬһ���ɾ��ķ�Һ���У����������ݳ��֣����շ�Һ�ʺ�ɫ���ɴ˲������ʣ� ������⣺��Һ�к�����Щ���ʣ�
�������ۣ���һ�����е����ʣ�ָʾ����ˮ�� ��
�ڻ�������ʹ��Һ�ʼ��Ե����ʣ���ʹ��Һ�ʼ��Ե�������ʲô��ͬѧ�������²��룮
С����Ϊ��ֻ��̼���ƣ���ʾ��̼����ˮ��ҺPH��7����С����Ϊ��ֻ���������ƣ�����Ϊ�������� ��
ʵ����ƣ�С�������Ȼ�����Һ����֤С����С������IJ��룮�������ϻ�Ϥ�Ȼ���
��Һ�����ԣ����������ʵ�飮���㽫С���ʵ����Ʋ���������
ʵ������ | Ԥ������ | Ԥ�ƽ��� |
ȡ������Һ�����ϲ���Һ���Թ��У���������Ȼ�����Һ�����ã� | ��û�а�ɫ��������Һ�ʺ�ɫ�� | �IJ�����ȷ�� |
���а�ɫ��������Һ�ɺ�ɫ��Ϊ��ɫ | �IJ�����ȷ�� | |
�� | ��IJ�����ȷ�� |
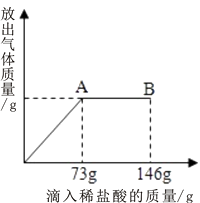
��4���ڼ�ʵ���У����������������Ϊ7.3%��ϡ����20.0gʱ����ʱ��Һ����ɫǡ���ɺ�ɫ��Ϊ��ɫ���Լ�������������Һ�����ʵ���������������ʾ������������Һ���ܶ�Ϊ1g/ml��
���𰸡�
��1������кͷ�Ӧ�Ƿ��ȷ�Ӧ�� NaOH+HCl=NaCl+H2O
��2���������ʹ�2NaOH+CO2=Na2CO3+H2O
��3���Ȼ��ƣ��������ƺ�̼���ƣ��а�ɫ����,��Һ�ʺ�ɫ��С����С��
��4���⣺������������Һ�����ʵ���������Ϊx��
NaOH+ | HCl=NaCl+H2O |
40 | 36.5 |
x��10g | 7.3%��20g |
40��36.5�T��x��10g������7.3%��20g��
x=16%
������������Һ�����ʵ���������Ϊ16%
���������⣺��1������������������к�����Ӧ��Һ�¶Ȳ����ߵģ���������������Ʒ����кͷ�Ӧ�����Ȼ��ƺ�ˮ�����Դ��ǣ�����кͷ�Ӧ�Ƿ��ȷ�Ӧ��NaOH+HCl=NaCl+H2O����2���������ƺͶ�����̼��Ӧ������̼���ƺ�ˮ��������ƿ�ڵ�ѹǿ��С��������ѹ���������Դ��ǣ��������ʹ�2NaOH+CO2=Na2CO3+H2O����3����������������Ʒ�Ӧ�����Ȼ��ƺ�ˮ�������̼���Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼�����Է�Ӧ��һ�������Ȼ��ơ�ˮ��ָʾ�������Դ��ǣ��Ȼ��ƣ�
���������ƺ�̼���ƶ��Լ��ԣ����Դ��ǣ��������ƺ�̼���ƣ�
�Ȼ��ƻ���̼���Ʒ�Ӧ����̼��Ƴ��������������Լ��ԣ���ʹ��̪���ɫ��
ʵ������ | Ԥ������ | Ԥ�ƽ��� |
ȡ������Һ�����ϲ���Һ���Թ��У���������Ȼ�����Һ�����ã� | ��û�а�ɫ��������Һ�ʺ�ɫ�� | С���IJ�����ȷ |
���а�ɫ��������Һ�ɺ�ɫ�� Ϊ��ɫ | С���IJ�����ȷ | |
���а�ɫ��������Һ�ʺ�ɫ | ��IJ�����ȷ |
�����㾫����������Ŀ����֪�����������кͷ�Ӧ����Ӧ�ú���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�����֪ʶ���Եõ�����Ĵ𰸣���Ҫ�����кͷ�Ӧ����������������κ�ˮ�ķ�Ӧ��ע�⣺a����ƽ b������ c�����ţ�

����Ŀ��ijͬѧ������ε�֪ʶ���������µ�������
��1����д�±��ո��еĻ�ѧʽ��
�Ȼ��� | �Ȼ��� | �Ȼ��� | �Ȼ�þ | �Ȼ��� | �Ȼ�п | �Ȼ����� | �Ȼ�ͭ |
KCl | CaCl2 | MgCl2 | AlCl3 | ZnCl2 | FeCl2 | CuCl2 |
��˼�������������еĽ���Ԫ�ص����У����Եó�������˳����������ģ�
��2��Ϊ����ϡ�����������������֮�䷢����Ӧ����ʵ�ʣ���������ͼ�������������ԲȦ�������ʵ��Ļ�ѧʽ�����ӷ��ţ�����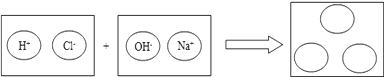
��3��ϡ�������������֮�䷢���ķ�Ӧ�ɳ�Ϊ��Ӧ��