题目内容
【题目】如图是初中化学中常用的实验装置,请回答下列问题。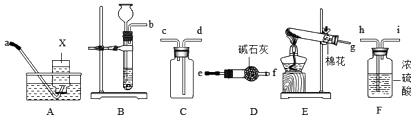
(1)仪器x的名称是;
(2)实验过程中经常要连接仪器。将玻璃导管插入带孔橡皮塞时,应先将要插入塞子的玻璃导管的一端 , 然后稍稍用力转动,使它插入带孔橡皮塞;
(3)实验室制取O2、CO2、H2均可选择(填装置代号)作为气体的发生装置;
(4)实验室不使用催化剂就能制取氧气的反应化学方程式为;若要制取纯度较高的氧气,应采用的收集方法是;
(5)请从以下装置(A至F间)选择并连接成一套组合装置,用于实验室制取干燥的二氧化碳气体。按照气体从左至右的流向写出所选装置小写字母接口的连接顺序:
()→()→()→()→……(可不填满,也可补充)
(6)将CO2和O2通入图N进行分离,最后当关闭阀门k,打开分液漏斗阀门时,收集到的气体是。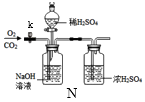
A.CO2、O2
B.CO2
C.O2
D.O2、H2O
(7)某小组学习“二氧化碳制取的研究”课题时,针对能不能用排水法收集CO2进行辩论,正方认为,不能用排水法收集二氧化碳,理由是:;反方认为能用排水法收集CO2 , 因为有措施可以减少CO2气体的溶解体积,你认为可行的措施之一是:。
【答案】
(1)集气瓶
(2)用水润湿
(3)B
(4)2KMnO4 ![]() K2MnO4 + MnO2 + O2↑,排水集气法
K2MnO4 + MnO2 + O2↑,排水集气法
(5)b,h,i,d
(6)B
(7)CO2 能溶于水,且会与水反应,改用温水(或加酸、事先制成CO2的饱和溶液等)
【解析】(1). 集气瓶(2).将玻璃导管插入带孔橡皮塞时,应先将要插入塞子的玻璃导管的一端用水湿润,以减小摩擦,然后稍稍用力转动,使它插入带孔橡皮塞(3).过氧化氢法制氧气,二氧化碳和氢气的制取所用药品都是固体和液体,反应条件都是常温,所以都可用固液常温型装置 B (4). 高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰、氧气,反应方程式为:2KMnO4 ![]() K2MnO4 + MnO2 + O2↑ (5). 排水集气法收集的气体较纯净 (6). 干燥二氧化碳应用浓硫酸,并长管进,短管出;二氧化碳应用向上排空气法收集;接口的连接顺序: ( b )→( h )→( i )→( d )→( )→( )→( ) (7). 打开分液漏斗阀门时,硫酸和碳酸钠反应生成二氧化碳,收集到的气体是 二氧化碳 (8). CO2 能溶于水,且会与水反应,不能用排水法收集;由于气体的溶解度随温度升高而减小,所以用排水法收集二氧化碳时可以改用温水(或加酸、事先制成CO2的饱和溶液等)以减少二氧化碳溶解的量。
K2MnO4 + MnO2 + O2↑ (5). 排水集气法收集的气体较纯净 (6). 干燥二氧化碳应用浓硫酸,并长管进,短管出;二氧化碳应用向上排空气法收集;接口的连接顺序: ( b )→( h )→( i )→( d )→( )→( )→( ) (7). 打开分液漏斗阀门时,硫酸和碳酸钠反应生成二氧化碳,收集到的气体是 二氧化碳 (8). CO2 能溶于水,且会与水反应,不能用排水法收集;由于气体的溶解度随温度升高而减小,所以用排水法收集二氧化碳时可以改用温水(或加酸、事先制成CO2的饱和溶液等)以减少二氧化碳溶解的量。
所以答案是:集气瓶、B、2KMnO4 ![]() K2MnO4 + MnO2 + O2↑、排水集气法、b、h、i、d、B、CO2 能溶于水,且会与水反应、改用温水(或加酸、事先制成CO2的饱和溶液等)。
K2MnO4 + MnO2 + O2↑、排水集气法、b、h、i、d、B、CO2 能溶于水,且会与水反应、改用温水(或加酸、事先制成CO2的饱和溶液等)。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】某兴趣小组在学习碱的化学性质时,进行了如图所示的实验. 
(1)在甲实验过程中,插入一支温度计来测量溶液的温度时,随着稀盐酸的不断滴入,溶液的温度逐渐升高,你认为溶液温度升高的原因是;写出该反应的化学方程式 .
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是;反应的化学方程式 .
(3)实验结束后,同学们将甲、乙两个实验的废液倒入同一个干净的废液缸中,看到有气泡出现,最终废液呈红色,由此产生疑问. 提出问题:废液中含有哪些物质?
交流讨论:①一定含有的物质:指示剂、水和 .
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想.
小兰认为:只有碳酸钠(提示:碳酸钠水溶液PH>7);小亮认为:只有氢氧化钠.你认为还可能是 .
实验设计:小斌想用氯化钙溶液来验证小兰、小亮和你的猜想.查阅资料获悉氯化钙
溶液呈中性,并设计如下实验.请你将小斌的实验设计补充完整.
实验内容 | 预计现象 | 预计结论 |
取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置. | ①没有白色沉淀,溶液呈红色. | 的猜想正确. |
②有白色沉淀,溶液由红色变为无色 | 的猜想正确. | |
③ | 你的猜想正确. |
(4)在甲实验中,如果消耗质量分数为7.3%的稀盐酸20.0g时,此时溶液的颜色恰好由红色变为无色,试计算氢氧化钠溶液中溶质的质量分数.(提示:氢氧化钠溶液的密度为1g/ml)
