题目内容
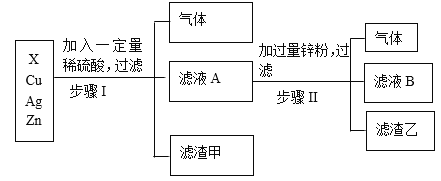
【题目】硫酸钙转化为K2SO4和CaCl2.6H2O的工艺流程如下:
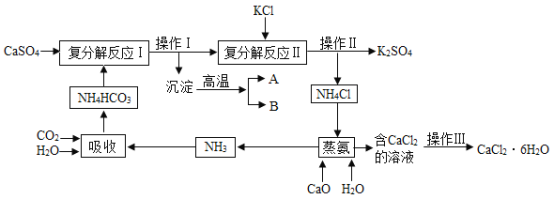
(1)操作I的名称为__________________________。
(2)蒸氨过程中完全没有涉及的反应类型为_____________(填编号)。
A 复分解反应
B 化合反应
C 分解反应
D 置换反应
(3)操作III包含一系列操作:蒸发浓缩、____________、过滤、洗涤、干燥。
【答案】过滤 CD 冷却结晶
【解析】
(1)碳酸氢铵与硫酸钙反应生成了碳酸钙沉淀和硫酸铵,是固液混合物,利用过滤的方法将它们分开;所以,操作I的名称为过滤;
(2)在蒸氨过程中,氧化钙与水化合生成了氢氧化钙,反应是:CaO+H2O═Ca(OH)2;该反应有两物质生成了一种物质,属于化合反应.氢氧化钙与氯化铵反应反应生成了氯化钙、氨气、水反应的方程式是:2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑,该反应有两种化合物相互交换成分生成了两种新的化合物,属于复分解反应,没有涉及到的反应是分解反应和置换反应,所以CD符合题意;
(3)从氯化钙溶液中结晶析出CaCl26H2O,需要:蒸发浓缩、冷却结晶、过滤、洗涤、干燥。

练习册系列答案
相关题目
【题目】某化学兴趣小组用化学方法测定一种钢样品中铁的含量,同学们称取了6.4g钢样品,投入装有50.0g稀盐酸的烧杯中恰好完全反应(假设样品中的其他物质不与酸反应)在实验过程中对烧杯(包括溶液和残余固体)进行四次称量,记录数据如下表:
反应时间/s | 0 | t1 | t2 | t3 |
烧杯和药品的质量/g | 85.4 | 85.3 | 85.2 | 85.2 |
请计算:
(1)反应生成氢气的质量为_____g。
(2)所用稀盐酸的溶质质量分数_____。