��Ŀ����
����Ŀ����ѧ��ȤС���ͬѧ����ij�������ķϼ�Һ����Ҫ�ɷ�Ϊ̼���ƣ������������Ȼ��ƣ��������ʲ��ƣ���ʯ����Ϊԭ���Ʊ��ռ�������õ��ռ�ֲ�Ʒ�ijɷֽ��з����Ͳⶨ��
�ֲ�Ʒ�Ʊ�
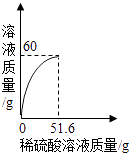
�ٽ��ϼ�Һ��������Ũ�����γɽ�Ũ����Һ����ȴ����ʯ�����ϣ�
�ڽ���Ӧ��Ļ������ˣ��õ�����Һ���������ᾧ���Ƶ�NaOH�ֲ�Ʒ��
��1���ֲ�Ʒ�ɷַ���
��ȡ�����ֲ�Ʒ����ˮ���μ�Ba��NO3��2��Һ���ְ�ɫ���ǣ��ôֲ�Ʒ��һ�������� �� ������ ��
�ڸ�С��ͬѧͨ���Դֲ�Ʒ�ɷֵ�ʵ�������ȷ���ôֲ�Ʒ�к����������ʣ�
��2���ֲ�Ʒ̼���ƺ����ⶨ
����ȤС���ͬѧ�������ͼ��ʾ��ʵ��װ�ã�ȡ10.0g�ֲ�Ʒ������ʵ�飮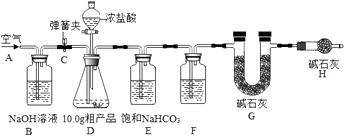
��������
�����Ӻ�װ�ã���������ԣ�
�ڴ��ɼ�C����A������ͨ��һ��ʱ�������
�۳���G������Ϊ12g��
�ܹرյ��ɼ�C�������μ�Ũ������������ֱ��D��������ð����
�ݴ��ɼ�C���ٴλ���ͨ��һ��ʱ�������
���ٴγ���G��������Ϊ13.48g��
������̽��
��F�е��Լ�ӦΪ �� Hװ�õ������� ��
����ʵ��10.0g�ֲ�Ʒֻ�ܲ���0.44g CO2 �� ����ϸ��������ʵ�飬ʵ��ֵ����ȷֵ0.44g���ƫ��ƫС������������ԭ�����������ȷ�� ��
���𰸡�
��1��Ca��OH��2��Ca��OH��2��Na2CO3�ܷ�����ѧ��Ӧ������Һ�в��ܹ���
��2��Ũ�����ֹ�����е�ˮ�Ͷ�����̼����Gװ�ã�ƫ��װ��D��Ũ����ӷ������Ȼ�����װ��E��NaHCO3��Ӧ����������̼
���������⣺�ֲ�Ʒ�ɷַ�����̼�����ܺ����ᱵ��Ӧ���ɳ�������ѧ����ʽΪ��Na2CO3+Ba��NO3��2=BaCO3��+2NaNO3�������ƺ�̼�����ܷ�Ӧ��
���Ca��OH��2��Ca��OH��2��Na2CO3�ܷ�����ѧ��Ӧ������Һ�в��ܹ��森
�ֲ�Ʒ�����ⶨ
Na2CO3�����IJⶨ����Ũ����������ˮ���������Ũ���ᣮ
Hװ���ܷ�ֹ�����еĶ�����̼��ˮ��������Gװ�ã������ֹ�����е�ˮ�Ͷ�����̼����Gװ�ã�����û��Hװ�ã���ⶨ�Ķ�����ֵ̼ƫ�ߣ����������������ƫ���ƫ��
װ��D��Ũ����ӷ������Ȼ�����װ��E��NaHCO3��Ӧ����������̼��ʹ������̼��ֵƫ���װ��D��Ũ����ӷ������Ȼ�����װ��E��NaHCO3��Ӧ����������̼��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�