题目内容
【题目】小丽同学取铜和氧化铜的混合物mg置于烧杯中,并向烧杯中逐滴加入稀硫酸溶液,不断搅拌,测得烧杯中溶液的质量与加入稀硫酸的质量关系如图所示.求: 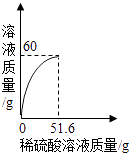
(1)mg混合物中,氧化铜的质量是克;
(2)当加入51.6g稀硫酸溶液时恰好完全反应,此时溶液中溶质的质量分数.
【答案】
(1)8.4
(2)解:设当加入51.6g稀硫酸溶液时恰好完全反应生成硫酸铜的质量为x.
H2SO4+ | CuO═ | CuSO4+H2O |
80 | 160 | |
8.4g | x |
![]()
x=16.8g
溶液中溶质的质量分数= ![]() ×100%=28%
×100%=28%
答:溶液中溶质的质量分数28%
【解析】解:(1)氧化铜和硫酸反应生成硫酸铜和水,而铜不和硫酸反应,所以溶液质量增加的就是氧化铜的质量,所以mg混合物中,氧化铜的质量=60g﹣51.6g=8.4g;故填:8.4;
(1)根据氧化铜和硫酸反应生成硫酸铜和水,而铜不和硫酸反应,所以溶液质量增加的就是氧化铜的质量进行解答;(2)根据溶液中溶质的质量分数= ![]() ×100%进行解答.
×100%进行解答.

练习册系列答案
相关题目