题目内容
【题目】100克某浓度的硫酸恰好与13克的锌完全起反应,请计算:
(1)生成氢气的质量(结果精确到0.1g).
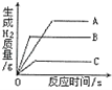
(2)将(1)的结果标在图中;
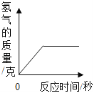
(3)反应后所得溶液中溶质的质量分数(写出计算过程,结果精确到0.1%).
【答案】(1)生成氢气的质量为0.4g;(2)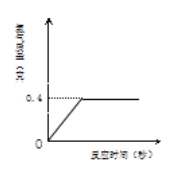 (3)所得溶液中溶质质量分数为28.6%。
(3)所得溶液中溶质质量分数为28.6%。
【解析】
试题分析:根据题意可知:反应为硫酸与锌反应生成氢气和硫酸锌。已知量为锌的质量为13g;未知量为(1)生成氢气的质量;(3)所得溶液中溶质质量分数。解题思路:(1)可根据锌与氢气的质量关系求解出生成氢气的质量。(3)可根据锌与硫酸锌的质量关系,求出生成硫酸锌(所得溶液中的溶质)的质量,再进一步根据溶质质量分数的计算方法求出所得溶液的溶质的质量分数。具体解题过程如下:
解:(1)设生成氢气的质量为x,生成硫酸锌的质量为y
Zn+H2SO4==ZnSO4+H2↑
65 161 2
13g y x
65:2=13g:x
x=0.4g
(3)65 :161=13g:y
y=32.2g
所得溶液中溶质的质量分数为:![]() ×100%≈28.6%
×100%≈28.6%
答:(1)生成氢气的质量为0.4g;
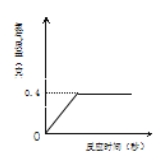
(2)
(3)所得溶液中溶质质量分数为28.6%。

练习册系列答案
相关题目