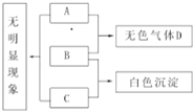
��Ŀ����
����Ŀ��С��ͬѧ�����껨��200Ԫ����һ��10g�ص���������п�Ͻ𣩣�����̽�������������ĺ����������뻯ѧ��ʦ����һ��̽������ʵ������������ϡ����ֶ����������ַ�Ӧ��ʵ�������±���
ϡ����/g | 10 | 10 | 10 | 10 | 10 |
ʣ���������/g | 8.7 | 7.4 | 6.1 | 4.8 | 4.8 |
�����ϱ��е����ݷ���������������⣺
��1�����С�������õ�������һö��ָ�����������������ٿˣ�
��2����������ϡ������������������Ƕ��٣�
���𰸡���1��4.8g��2��19.6%
��������
�����������1���Ƚϵ��Ĵκ͵���ε����ݿ���֪����ʣ������������Ϊ4.8g������˵���ù�������������4.8g��С�������õ�������һö��ָ��������������4.8g��
��2����ϡ��������������Ϊx��������п������Ϊ��10g��4.8g=5.2g
Zn+H2SO4�TZnSO4+H2��
65 98
5.2g x
![]()
x=7.84g
����ϡ������������������ǣ�![]() =19.6%
=19.6%
�𣺣�1��С�������õ�������һö��ָ��������������4.8g
��2������ϡ�������������������19.6%

��ϰ��ϵ�д�
 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
�����Ŀ