题目内容
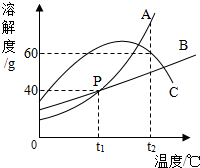 如图所示为A、B、C三种可溶物的溶解度曲线.结合图示回答以下问题.
如图所示为A、B、C三种可溶物的溶解度曲线.结合图示回答以下问题.(1)图中点P表示的意义是
(2)t2℃时A、B、C三种物质的溶解度由小到大的顺序为
(3)t1℃时将25g B物质放入50g水中,所得溶液的溶质质量分数为
(4)欲从A溶质的饱和溶液中得到A晶体,通常采用的方法是
(5)下列说法不正确的是
①t2℃时A、B、C三种溶质的溶液浓度由大到小的顺序是A>B>C
②将t2℃时A、B、C三种溶质的饱和溶液降温到t1℃,三者均有晶体析出
③将接近饱和的B溶质溶液转化为饱和溶液可以通过恒温蒸发溶剂的方法
④改变C溶质饱和溶液的温度时,一定有晶体析出.
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,饱和溶液和不饱和溶液相互转变的方法,晶体和结晶的概念与现象,有关溶质质量分数的简单计算
专题:溶液、浊液与溶解度
分析:根据溶解度曲线即可知道在不同温度下各物质的溶解度,根据溶质质量分数=
×100%,根据溶解度随温度的变化特点确定结晶的方法,据此解答.
| 溶质质量 |
| 溶液质量 |
解答:解:(1)P点表示在t1℃时AB两种物质的溶解度相等,故填:在t1℃时AB两种物质的溶解度相等;
(2)据图可以看出,在t2℃时A、B、C三种物质的溶解度由小到大的顺序为BCA,故填:BCA;
(3)t1℃时B物质的溶解度是40g,将25g B物质放入50g水中,只能溶解20g,所得溶液的溶质质量分数为
×100%≈28.6%,故填:28.6%;
(4)据图可以看出,A物质的溶解度随温度升高变化大,故从A溶质的饱和溶液中得到A晶体,通常采用的方法是冷却热的饱和溶液,故填:冷却热的饱和溶液;
(5)①t2℃时,A、B、C三种溶质的饱和溶液浓度由大到小的顺序是A>B>C,错误;
②将t2℃时,A、B、C三种溶质的饱和溶液降温到t1℃,C溶液没有晶体析出,错误;
③将接近饱和的B溶质溶液转化为饱和溶液可以通过恒温蒸发溶剂的方法,正确;
④改变C溶质饱和溶液的温度时,不一定有晶体析出;
故填:①②④.
(2)据图可以看出,在t2℃时A、B、C三种物质的溶解度由小到大的顺序为BCA,故填:BCA;
(3)t1℃时B物质的溶解度是40g,将25g B物质放入50g水中,只能溶解20g,所得溶液的溶质质量分数为
| 20g |
| 70g |
(4)据图可以看出,A物质的溶解度随温度升高变化大,故从A溶质的饱和溶液中得到A晶体,通常采用的方法是冷却热的饱和溶液,故填:冷却热的饱和溶液;
(5)①t2℃时,A、B、C三种溶质的饱和溶液浓度由大到小的顺序是A>B>C,错误;
②将t2℃时,A、B、C三种溶质的饱和溶液降温到t1℃,C溶液没有晶体析出,错误;
③将接近饱和的B溶质溶液转化为饱和溶液可以通过恒温蒸发溶剂的方法,正确;
④改变C溶质饱和溶液的温度时,不一定有晶体析出;
故填:①②④.
点评:本题考查了溶解度曲线的意义和应用,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 2014年5月9日南京市江北某厂区丢失放射性源铱-192,由于丢失的放射性源铱-192属于二类放射源,对人体有很大的辐射危害,下列关于铱的说法正确的是( )
2014年5月9日南京市江北某厂区丢失放射性源铱-192,由于丢失的放射性源铱-192属于二类放射源,对人体有很大的辐射危害,下列关于铱的说法正确的是( )| A、铱的原子核内有77中子 |
| B、铱是非金属元素 |
| C、铱的相对原子质量是192.22g |
| D、铱的原子核外有77个电子 |


 ”和“
”和“ ”,反应后的“
”,反应后的“ ”各粒子间的个数比为
”各粒子间的个数比为