题目内容
【题目】酸,碱,盐是有广泛用途的重要化学物质.试完成下列人关探究.
(1)实验室里有一瓶敞口放置的浓盐酸,它的质量分数与放置天数的关系如图A所示.假设水不蒸发,分析浓盐酸的溶质质量分数变化的原因为____.
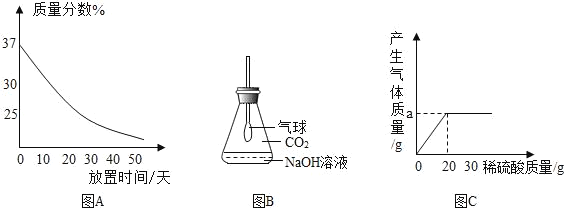
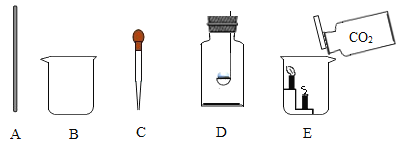
(2)观察图B中的装置,向事先收集满CO2气体的锥形瓶中倒入一定量的氢氧化钠溶液,塞紧瓶塞振荡,可观察到的现象是_____.
(3)馒头、面包等发面食品松软可口,它们有一个共同特点是面团中有许多小孔.根据发酵粉(含碳酸氢钠和有机酸等)可与面粉、水混合直接制作发面食品的事实,说明碳酸氢钠在其中的作用为____.
(4)在常温下将HCl、NaCl、NaOH、Ca(OH)2、Na2CO3等几种溶液两两混合.
①当HCl与NaOH或Ca(OH)2溶液后,虽然发生了反应,但观察不到明显现象.请你设计一个实验方案证明它们确实发生了化学反应._____
②若混合后溶液的质量减少,试写出所有可能的组合_____.
③将溶质质量分数为19.6%的稀硫酸逐滴加入Na2CO3溶液中,若产生气体质量与加入稀硫酸的质量有如图C所示关系,则a的数值为_____.
【答案】浓盐酸具有挥发性,HCl气体挥发,导致溶质减少,溶质质量分数减少 气球膨胀 碳酸氢钠与有机酸反应,产生大量二氧化碳气体,留下气孔,使面食松软可口 实验方案为:向氢氧化钠或氢氧化钙溶液中滴加无色酚酞溶液,然后再向其中加入稀盐酸,若观察到溶液由红色逐渐变为无色,则证明发生了化学反应 Na2CO3和HCl、Na2CO3和Ca(OH)2 1.76g
【解析】
氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸氢钠和酸反应生成盐、水和二氧化碳,碳酸钠和盐酸反应能生成氯化钠、水和二氧化碳,碳酸钠和氢氧化钙反应生成氢氧化钠和碳酸钙沉淀。
(1)浓盐酸的溶质质量分数变化的原因是:浓盐酸具有挥发性,HCl气体挥发,导致溶质减少,溶质质量分数减少。
(2)氢氧化钠溶液吸收二氧化碳后,锥形瓶中的压强减小,可观察到气球膨胀起来。
(3)碳酸氢钠在其中的作用是:碳酸氢钠与有机酸反应,产生大量二氧化碳气体,留下气孔,使面食松软可口。
(4)①实验方案为:向氢氧化钠或氢氧化钙溶液中滴加无色酚酞溶液,然后再向其中加入稀盐酸,若观察到溶液由红色逐渐变为无色,则证明发生了化学反应。
②Na2CO3和HCl混合时,碳酸钠和盐酸反应能生成氯化钠、水和二氧化碳,二氧化碳从溶液中逸出,溶液质量减小。
Na2CO3和Ca(OH) 2混合时,碳酸钠和氢氧化钙反应生成氢氧化钠和碳酸钙沉淀,碳酸钙从溶液中析出,溶液质量减小。
③
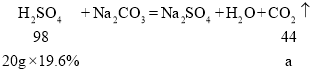
![]()
![]()
故a的数值是1.76g.