题目内容
【题目】2018年5月9日,我国“高分五号”卫星发射成功。
(1)高氯酸钾(KClO4)可用作火箭燃料,其中氯元素的化合价为_______。
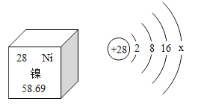
(2)“高分五号”用钛镍形状记忆合金制作卫星天线。如图是镍元素在元素周期表中的信息以及原子结构示意图。则镍元素位于元素周期表的第____周期,x的数值是_______。
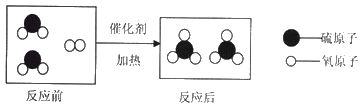
(3)“高分五号”是我国首颗对大气中二氧化硫,二氧化氮.甲烷(CH4)等多个环境要素进行监测的卫星。催化还原法是消除大气中氮氧化物污染的新工艺,主要的微观示意图如下:

①请写出图示反应的化学方程式:______________;
②下列有关说法正确的是_________(填序号)。
A.反应前后元素和原子的种类和个数不变 B.反应前后分子的种类发生改变
C.反应前后元素化合价都不变 D.丙是由两个氮原子构成的 E.反应生成的戊.丁的质量比为11:9
【答案】+7 4 2 CH4+2NO2![]() N2+2H2O+CO2 BE
N2+2H2O+CO2 BE
【解析】
(1)在高氯酸钾(KClO4)中钾元素的化合价为+1价,氧元素的化合价为-2价,设:氯元素的化合价为x,根据化合物中各元素化合价的代数和为零,则有:(+1)+x+(-2)×4=0,x=+7;
(2)根据镍原子的结构示意图可知,该原子核外有4个电子层,在元素周期表中,周期数等于电子层数,所以位于元素周期表的第四周期;在原子中,核内质子数等于核外电子数,可推出X的数值是:28-2-8-16=2;
(3)①由微粒的结构示意图可知,在一定条件下,参加反应的物质是CH4和NO2,生成的物质是N2、H2O和CO2,该反应的化学方程式是:CH4+2NO2![]() N2+2H2O+CO2;
N2+2H2O+CO2;
②A、由微粒的变化可知,反应前后原子的种类没有发生改变,元素只讲种类,不论个数,故A错误;
B、由微粒的变化可知,反应前后分子的种类发生了变化,故B正确;
C、该反应有单质(氮气)生成,单质的化合价为零,NO2中氮元素的化合价为+4价,反应前后元素一定有化合价的变化,故C错误;
D、由方程式可知,丙是氮气,氮气是由氮分子构成,1个氮分子是由两个氮原子构成,故D错误;
E、由方程式可知,反应后戊、丁的质量比=44:(2×18)=11:9,故E正确。故选BE。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【题目】某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰。该小组同学进行了如下探究。
(1)写出铁丝在氧气中燃烧的化学式表达式:_________。
(2)探究一:蜡烛燃烧产生火焰的原因是什么?
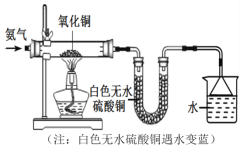
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,
也有火焰产生(如图所示)。
![]()
由此可知:蜡烛燃烧产生的火焰是由气态物质燃烧形成的。
(3)探究二:物质燃烧产生火焰的根本原因是什么?
(查阅资料)
物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50∽70 | 300∽550 | 约600 |
铁 | 1535 | 2750 | 越1800 |
钠 | 97.8 | 883 | 越1400 |
由上表可知:物质燃烧能否产生火焰与其________________(填“熔点”或“沸点”)和燃烧时温度有关。由此推测:钠在燃烧时,____________(填“有”或“没有”)火焰产生。
【题目】稀土是一种重要的战略资源。铈是一种常见的稀土元素,下列有关铈的说法正确的是
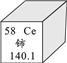
A. 铈属于非金属元素
B. 铈原子的中子数是58
C. 铈原子的核外电子数是58
D. 铈原子的相对原子质量是140.1g
【题目】3.0g某物质完全燃烧后生成4.4gCO2和1.8g水.则对该物质相关判断正确的是( )
| A. | 该物质只含碳、氢元素 |
| B. | 该物质一定含有碳、氢元素,可能含有氧元素 |
| C. | 该物质由碳、氢、氧元素组成 |
| D. | 该物质分子中碳原子和氢原子的个数比为1:1 |