题目内容
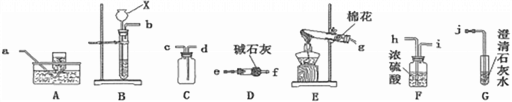
【题目】下列实验操作中,正确的是( )
A. 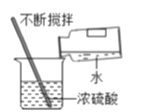 稀释浓硫酸 B.
稀释浓硫酸 B. 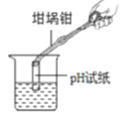 测溶液的pH C.
测溶液的pH C.  称量固体 D.
称量固体 D.  加热液体
加热液体
【答案】D
【解析】A、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中,操作错误;B、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH,不能将pH试纸伸入待测液中,以免污染待测液,操作错误;C、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,操作错误;
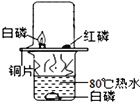
D、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的1/3,操作正确。故选D。

 阅读快车系列答案
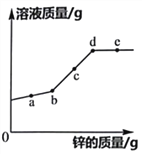
阅读快车系列答案【题目】下列图象不能正确反映对应变化关系的是( )
|
|
|
|
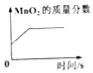
A.向盛有NaOH溶液的烧杯中滴加稀盐酸 | B.加热氯酸钾和二氧化锰的固体混合物 | C.在一定温度下,向接近饱和的氯化钾溶液中加入氯化钾固体 | D.将质量相等的镁粉和锌粉分别加入到足量且质量分数相等的稀硫酸中 |
【题目】下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 42 | 109 | 129 | 174 | 314 | 347 | |
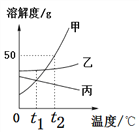
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中能表示Ca(OH)2溶解度曲线的是_______(填“A”或“B”)。
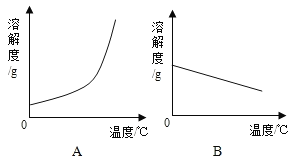
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,有下列措施:①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度。其中均可行的一组是______(填序号)
A.①②④ B.②③④ C.①③⑤ D.①②⑤
(3)20℃时,200g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH晶体的质量为________g。
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量的CaO固体后,恢复到20℃,得到的溶液(乙溶液),已知:CaO + H2O = Ca(OH)2 。 则甲乙溶液中溶质的质量分数的关系为ω(乙)_____ω(甲)(填“>”、“<”或“=”)。
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是________。