题目内容
【题目】核电荷数为1~18的元素的原子结构示意图等信息如下,请回答下列问题上。
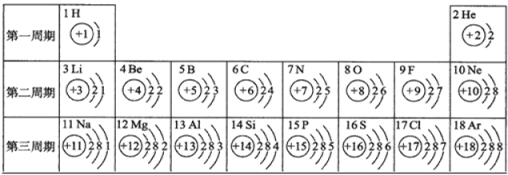
(1)第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是__________。
(2)用上表中给出的元素,写出含有氮元素的常见单质、化合物的化学式各一个,
并标出所写化学式中氮元素的化合价:单质__________、化合物__________。
(3)1号元素和6号元素组成的甲烷(CH4),在自然界中有广泛存在。2017年5月我国首次海域可燃冰试采成功。可燃冰外观像冰,主要含有甲烷水合物(由甲烷分子和水分子组成),还含有少量二氧化碳等物质。
①可燃冰属于___________(填“纯净物”或“混合物”)。
②科学家在较低的温度和压力下,用甲烷等为原料制成了金刚石薄膜,该变化属于_________(填“物理变化”或“化学变化”)。
③甲烷(CH4)可用作燃料,甲烷在空气中完全燃烧生成二氧化碳和水写出该反应的化学式表达式: ___________。
④常温常压时,若甲烷和以下选项中两种气体组成的混合物中,碳元素的质量分数为80%,则另两种气体可能是___________。
H2和CO B.H2和C2H2 C.CO和C2H4
【答案】最外层电子从左向右顺序递增 ![]()
![]() 混合物 化学变化 CH4+2O2
混合物 化学变化 CH4+2O2![]() CO2+2H2O B、C
CO2+2H2O B、C
【解析】
(1)第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是由左至右依次递增;
(2)含有氮元素的常见单质是氮气,氮气中氮元素化合价是0,可以表示为![]() ;含有氮元素的常见化合物有二氧化氮,二氧化氮中氮元素化合价是+4,可以表示为
;含有氮元素的常见化合物有二氧化氮,二氧化氮中氮元素化合价是+4,可以表示为![]() ;
;
(3)①可燃冰中含有多种物质,属于混合物;
②科学家在较低的温度和压力下,用甲烷等为原料制成了金刚石薄膜,属于化学变化;
③甲烷在空气中完全燃烧生成二氧化碳和水,反应的化学方程式为:CH4+2O2![]() CO2+2H2O;
CO2+2H2O;
④甲烷中碳元素质量分数为:![]() ×100%=75%,
×100%=75%,
一氧化碳中碳元素质量分数为:![]() ×100%<80%,
×100%<80%,
乙炔中碳元素质量分数为:![]() ×100%>80%,
×100%>80%,
乙烯中碳元素质量分数为:![]() ×100%>80%,
×100%>80%,
由以上分析可知,常温常压时,若甲烷和以下选项中两种气体组成的混合物中,碳元素的质量分数为80%,则另两种气体可能是H2和C2H2、CO和C2H4。