题目内容
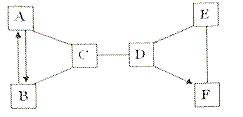
【题目】向一定量盐酸和氯化铁溶液的混合物中逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是( )
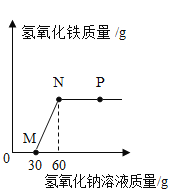
A. M点表示的溶液中只含有一种溶质
B. N点表示的溶液pH=7
C. P点和N点表示的溶液中,NaC1的质量分数相同
D. 从M点到N点溶液质量增加30g
【答案】B
【解析】
A、M点表示加入的氢氧化钠与盐酸恰好完全中和生成氯化钠和水,氯化铁还没有参与反应,所以此时溶液中的溶质是氯化钠和氯化铁两种,故错误;
B、N点表示的溶液是氢氧化钠恰好与氯化铁完全反应生成氯化钠和氢氧化铁沉淀,此时溶液中只有一种溶质﹣﹣氯化钠,溶液显中性,即pH=7,故正确;
C、N点表示的氯化铁和氢氧化钠恰好完全反应,P点表示氯化铁和氢氧化钠恰好完全反应后,又增加了一定量的氢氧化钠溶液,两部分中氯化钠的量是一定的,所以P点表示的溶液比N点表示的溶液中氯化钠的质量分数小,故错误;
D、从M点到N点是增加了30g,但由化学方程式FeCl3+3NaOH=Fe(OH)3↓+3NaCl可知,溶液应增加少于30g,故错误。
故选B。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案【题目】某化学小组为验证稀硫酸的性质,并探究反应后废液的成分,进行了如下实验。
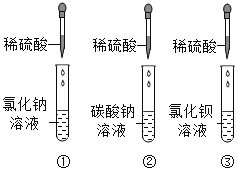
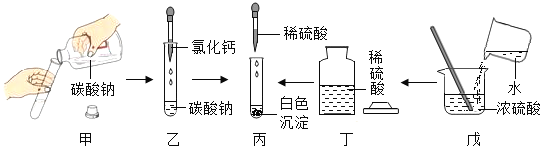
I:验证稀硫酸的某些性质
(1)按图所示进行实验,其中试管_____(选填序号)中无明显现象,小组同学讨论认为该试管中的两种物质间没有发生复分解反应,他们的理由是_____。
(2)为验证稀硫酸和氢氧化钠溶液是否发生反应,小明和小红分别向盛有氢氧化钠溶液的试管中,先加稀硫酸,再向混合后的溶液中滴加几滴酚酞溶液,结果小明观察到溶液为红色。小红观察到溶液为无色,于是二者得出了不同的结论。
小组同学在不改变所用试剂的情况下。对他们的实验方案进行了修改,从而确保实验一定能得出“硫酸与氢氧化钠溶液发生了化学反应”的结论。他们的实验方案是(只写操作过程):_____。
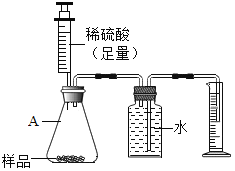
Ⅱ:探究反应后废液的成分
将如图所示实验后三支试管中的物质均倒入同一烧杯中,充分混合后静置,得到白色沉淀和无色溶液,用pH计测得无色溶液的pH=8.6。
(提出问题)无色溶液中溶质的成分是什么?
(作出猜想)猜想一:Na2CO3和NaCl;猜想二:H2SO4和Na2SO4;
猜想三:NaCl和Na2SO4;猜想四:Na2CO3、NaC1和Na2SO4
小组讨论认为猜想二不合理,理由是_____。
(进行实验)
实验步骤 | 实验操作 | 实验现象 | 实验结论 |
① | 取少量无色溶液于试管中。向其中滴加稀盐酸 | _____ | 猜想三不成立 |
② | 向步骤①后的溶液中加入BaCl2溶液。 | 产生白色沉淀 | 猜想四成立 |
小组同学认为“猜想四成立”这一结论是不可靠的,理由是_____。(用化学方程式表示)。
小组同学在不改变所用试剂的情况下,对实验方案进行了修改,并重新进行了实验,仍然得出“猜想四成立”的结论。他们修改后的实验方案是_____。