题目内容
【题目】侯德榜是我国著名的化学家。由他发明的侯氏制碱法制得的纯碱中含有少量氯化钠杂质。某化学兴趣小组的同学为了测定该厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计了如下两种实验方案
方案一:称取样品10.65g,加水完全溶解,向其中加入足量的氯化钡溶液,发生如下反应Na2CO3+BaCl2=BaCO3↓+2NaCl
充分反应后,过滤、洗涤,干燥得固体19.70g.通过计算(写出计算过程)判断该厂的产品是否属于优等品。(杂质可溶于水且不与氯化钡反应)
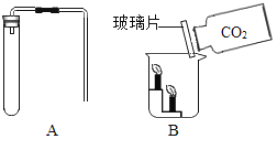
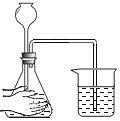
方案二:用如图所示的装置,通过准确测量排出水的体积,也可计算样品的纯度。称取纯碱固体2.0g,加入足量的稀硫酸,发生如下反应:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,完全反应,使气体放出,测得量筒中水的体积为330毫升,请你计算样品的纯度(本题中二氧化碳的密度取2.0g/L)
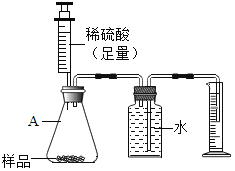
(1)请任意选择一种方案进行计算。________
(2)同学分析发现方案二所测的碳酸钠纯度偏低,造成此结果的原因可能是______(装置的气密性良好)
A A装置中残留反应产生的二氧化碳气体 B 部分CO2溶于水或与水反应
C 与量筒相连的导管中有水 D 量筒读数时,俯视读数。
【答案】按方案一计算:纯碱属于优等品;
按方案二计算:纯碱不属于优等品 ABC
【解析】
(1)利用方案一进行计算:
设碳酸钠质量为x,

![]() =
=![]() ,
,
x=10.6g,
碳酸钠质量分数为:![]() ×100%=99.5%,
×100%=99.5%,
通过计算可知,该厂生产的纯碱属于优等品。
利用方案二计算:
设碳酸钠质量为y,
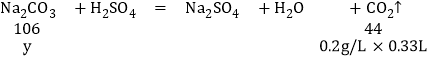
![]() =
=![]() ,
,
y=1.59g,
碳酸钠质量分数为:![]() ×100%=79.5%,
×100%=79.5%,
通过计算可知,该厂生产的纯碱不属于优等品。
(2)A装置中残留反应产生的二氧化碳气体,部分CO2溶于水或与水反应,与量筒相连的导管中有水,都能够导致测定结果偏低,量筒读数时,俯视读数,会导致测定结果偏高。
故选:ABC。

 阅读快车系列答案
阅读快车系列答案