题目内容
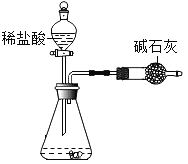
【题目】某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空:
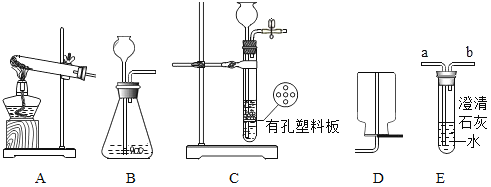
(1)收集某气体只能采用D装置,由此推测该气体具有的性质_____;
(2)写出实验室用A装置制取氧气的化学方程式____;
(3)制取气体时,让反应随时停止应选择的气体发生装置是____;(填字母)
(4)实验室制取二氧化碳应选择的气体发生装置是____ (填字母) ,化学反应原理____,验证生成的气体是二氧化碳时,应将气体从____(填“a”或“b”)口进入E中。
【答案】密度比空气小,易溶于水 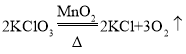 C B CaCO3+2HCl=CaCl2+H2O+CO2↑ a
C B CaCO3+2HCl=CaCl2+H2O+CO2↑ a
【解析】
(1)D装置是向下排空气法,若能使用D装置则证明气体的密度小于空气。而只能用D说明收集该气体无法使用排水法收集,原因是该气体易溶于水。故答案为:密度比空气小,易溶于水;
(2)实验室使用A装置制取氧气,A装置是固固加热法,实验室使用固固加热法制取氧气的实验方法有两种,一种是加热高锰酸钾,一种是加热氯酸钾和二氧化锰的混合物。而二者的区别是,利用高锰酸钾制取氧气需要在试管口放一团棉花,而氯酸钾不需要。故A装置描述的是氯酸钾制取氧气。故答案为: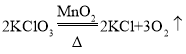 ;
;
(3)制取气体时,C装置可以随时控制反应的发生与停止。若要让装置发生化学反应,则打开弹簧夹,受到气压的影响,液体流下,和带孔隔板上的固体接触从而制取气体,若要停止反应,则关闭弹簧夹,气体在试管内累积,试管内的压强增大,液体被压入长颈漏斗下端管口中,固体和液体无法接触,反应停止。故答案为:C;
(4)实验室使用固体药品块状大理石和液体药品稀盐酸在常温的状态下混合制取二氧化碳,故选择的发生装置应该是固液混合不加热发,即实验装置B。其反应原理是大理石中的主要成分碳酸钙和稀盐酸中的溶质氯化氢反应生成氯化钙、水和二氧化碳,故其化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑。验证生成的二氧化碳,需要使用澄清的石灰水,澄清的石灰水遇到二氧化碳会变浑浊,为了使二者充分接触,反应更为完全,现象更明显,应该将二氧化碳气体从装置E中的长管a通入。故答案为:B、CaCO3+2HCl=CaCl2+H2O+CO2↑、a。

【题目】下列实验设计能达到实验目的的是( )
选项 | 实验目的 | 实验设计 |
A | 除去CO中的少量 | 先通过浓硫酸再通过氢氧化钠溶液 |
B | 除去铁粉中的铜粉 | 加入足量的稀 |
C | 除去 | 加入适量的 |
D | 鉴别 | 加入适量 |
A.AB.BC.CD.D
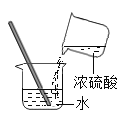
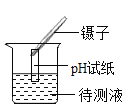
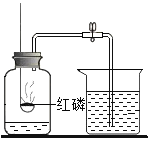
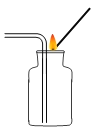
【题目】小杰同学在复习铁生锈条件时知道,常温下,没有氧气,铁与水几乎不反应。老师告诉同学们,高温下,铁与水蒸气能反应生成一种常见的铁的氧化物和一种气体。小杰很好奇,设计如图所示实验探究铁粉与水蒸气反应后的产物。
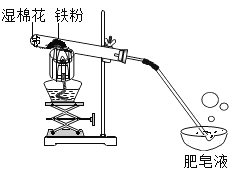
(1)试管尾部放一团湿棉花的目的是___________________。
(2)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是_________________。
(3)探究试管中剩余固体成分是什么?
(查阅资料)常见的铁的氧化物有FeO(黑色、没有磁性)、![]() 、
、![]() 。
。
(初步验证)试管中固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是![]() ;猜想二剩余固体是__________________。
;猜想二剩余固体是__________________。
(实验探究)
实验操作 | 实验现象结论 |
______________________ | ___________________证明猜想一正确 |
(实验结论)铁和水蒸气反应的化学方程式:___________________。
(反思与交流)该黑色固体不可能是![]() ,理由是___________________。
,理由是___________________。