题目内容
【题目】某同学对“菠菜中富含可溶性草酸盐和碳酸盐,与豆腐同食会引起结石”的说法产生了兴趣。
探究:菠菜里是否含有可溶性草酸盐和碳酸盐?
【查阅资料】
①可溶的草酸盐、碳酸盐能与CaCl2溶液反应生成难溶于水的草酸钙(CaC2O4)、碳酸钙。
②醋酸(化学式用HAc表示)不与草酸钙反应,但能与碳酸钙反应生成可溶性盐。
【实验流程】
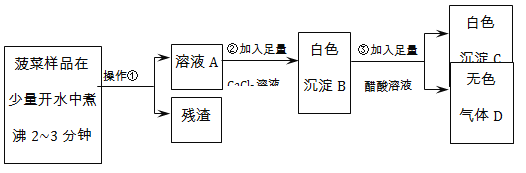
根据流程回答问题:
(1)操作①的名称是______________________________________。
(2)加入足量CaCl2溶液的目的是____________________________________。
(3)已知气体D能使澄清石灰水变浑浊,步骤③中发生反应的化学反应方程式为____。
【答案】 过滤 将溶液中的草酸根和碳酸根完全沉淀出来 CaCO3 + 2HAc = Ca(Ac)2 + H2O + CO2↑
【解析】探究:菠菜里是否含有可溶性草酸盐和碳酸盐?【查阅资料】①可溶的草酸盐、碳酸盐能与CaCl2溶液反应生成难溶于水的草酸钙(CaC2O4)、碳酸钙。②醋酸(化学式用HAc表示)不与草酸钙反应,但能与碳酸钙反应生成可溶性盐。【实验流程】(1)操作①的名称是过滤,把不溶于液体的固体物质过滤出来。(2)加入足量CaCl2溶液的目的是将溶液中的草酸根和碳酸根完全沉淀出来,草酸盐、碳酸盐能与CaCl2溶液反应生成难溶于水的草酸钙(CaC2O4)、碳酸钙。(3)已知气体D能使澄清石灰水变浑浊,步骤③中发生反应的化学反应方程式为CaCO3 + 2HAc = Ca(Ac)2 + H2O + CO2↑,醋酸(化学式用HAc表示)不与草酸钙反应,但能与碳酸钙反应生成可溶性盐。
点睛∶可溶的草酸盐、碳酸盐能与CaCl2溶液反应生成难溶于水的草酸钙(CaC2O4)、碳酸钙。醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐。

 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案【题目】钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)下列铁制品的利用与金属导热性有关的是_________________
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的_______。
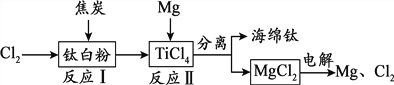
II.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:______________;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能____________。
Ⅲ.铁的活动性探究
现用一定量的AgNO3和Cu (NO3)2混合溶液,进行了如下图所示的实验,并对溶液A和固体B的成分进行了分析和研究.
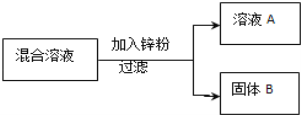
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】
①只有Zn(NO3)2
②有Zn(NO3)2、AgNO3
③有Zn(NO3)2、Cu(NO3)2
④有Zn(NO3)2、Cu(NO3)2、AgNO3
【交流讨论】不合理的猜想是_______(填标号),其理由是__________
【实验探究】根据如表中的实验步骤及现象,完成表中的实验结论
实验步骤 | 现象 | 实验结论 |
取少量固体B,滴加稀盐酸 | 有气泡产生 | 溶液A中的溶质成分符合猜想__, 固体B中的金属成分有________种. |
Ⅳ.生铁中铁含量的测定
某课外兴趣小组测定生铁(含杂质的铁,杂质既不溶于水也不溶于酸)中铁的质量分数,他们取五份样品,分别加稀硫酸反应.测得部分数据如下,请根据有关信息回答问题.
实验次数 | 1 | 2 | 3 | 4 | 5 |
取样品质量(g) | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 |
取稀硫酸质量(g) | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
产生气体质量(g) | 0.2 | a | 0.6 | 0.8 | 0.9 |
(1)a的数值为_______________.
(2)第5次实验结束后,所得到溶液中溶质的化学式为_________________.
(3)列式计算该样品中单质铁的质量分数是______________。
(4)所用稀硫酸的溶质的质量分数为____________。