题目内容
【题目】钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)下列铁制品的利用与金属导热性有关的是_________________
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的_______。
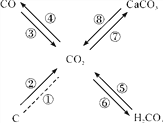
II.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:______________;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能____________。
Ⅲ.铁的活动性探究
现用一定量的AgNO3和Cu (NO3)2混合溶液,进行了如下图所示的实验,并对溶液A和固体B的成分进行了分析和研究.
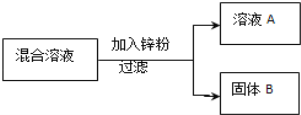
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】
①只有Zn(NO3)2
②有Zn(NO3)2、AgNO3
③有Zn(NO3)2、Cu(NO3)2
④有Zn(NO3)2、Cu(NO3)2、AgNO3
【交流讨论】不合理的猜想是_______(填标号),其理由是__________
【实验探究】根据如表中的实验步骤及现象,完成表中的实验结论
实验步骤 | 现象 | 实验结论 |
取少量固体B,滴加稀盐酸 | 有气泡产生 | 溶液A中的溶质成分符合猜想__, 固体B中的金属成分有________种. |
Ⅳ.生铁中铁含量的测定
某课外兴趣小组测定生铁(含杂质的铁,杂质既不溶于水也不溶于酸)中铁的质量分数,他们取五份样品,分别加稀硫酸反应.测得部分数据如下,请根据有关信息回答问题.
实验次数 | 1 | 2 | 3 | 4 | 5 |
取样品质量(g) | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 |
取稀硫酸质量(g) | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
产生气体质量(g) | 0.2 | a | 0.6 | 0.8 | 0.9 |
(1)a的数值为_______________.
(2)第5次实验结束后,所得到溶液中溶质的化学式为_________________.
(3)列式计算该样品中单质铁的质量分数是______________。
(4)所用稀硫酸的溶质的质量分数为____________。
【答案】 B 氧气和水 略 提供热量 ② 因为银的金属活动性顺序最弱,锌先置换溶液中的银后置换溶液中的铜,故溶液中若有硝酸银就一定会有硝酸铜存在(意思正确即可) ① 3 0.4 FeSO4和H2SO4 84% 19.6%
【解析】I(1)物质的性质决定了物质的用途,所以可以根据铁的用途,分析利用了铁的什么性质;(2)根据铁锈蚀的条件分析;II(1)冶炼铁的主要原料是铁矿石、焦炭、空气等物质,通过反应生成的一氧化碳可以把铁矿石中的铁还原出来;(2)根据高炉炼铁的原料及各原料的作用分析即可;Ⅲ【交流讨论】根据已有的金属活动性顺序的意义进行分析解答,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此解答;【实验探究】根据金属与酸反应的现象分析解答;Ⅳ(1)(2)由表中数据分析解答;(3)根据样品完全反应生成气体的质量计算出铁的质量,从而求解样品中铁的质量分数;(4)根据第1次实验生成气体的质量求解消耗稀硫酸中溶质的质量,从而求解稀硫酸的溶质质量分数。I(1)分析所给三种金属制品可以知道,铁锅是利用了金属的导热性,故选B;(2)铁吸收水与氧气后会变成铁锈,所以“双吸剂”它能够吸收空气中的水分和氧气;II(1)赤铁矿的主要成分是氧化铁,氧化铁和一氧化碳反应能生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO高温2Fe+3CO2;(2)炼铁时要用到焦炭,它有两个作用。炼铁时需要高温,焦炭与氧气反应生成二氧化碳,同时放出大量热,可供给炼铁使用;炼铁时还需一氧化碳作还原剂,二氧化碳与过量焦炭反应可以生成一氧化碳;Ⅲ【交流讨论】不合理的猜想是②,其理由是因为银的金属活动性顺序最弱,锌先置换溶液中的银后置换溶液中的铜,故溶液中若有硝酸银就一定会有硝酸铜存在;【实验探究】取少量固体B,滴加稀盐酸,有气泡产生,说明固体B中含有锌,同时说明所加锌过量,将溶液中的银、铜全部置换出来。溶液A中的溶质成分是Zn(NO3)2。符合猜想①;固体B中的金属成分有过量的锌及被置换出来的铜和银共3种;Ⅳ(1)由表中数据可知,反应开始时,每50g稀硫酸与样品反应产生0.2g气体。故a值为0.4;(2)第5次实验结束后共产生气体0.9g,表示样品反应完,稀硫酸有剩余。故所得到溶液中溶质的化学式为FeSO4和H2SO4;
(3)设样品中铁的质量为x。
Fe+ H2SO4 =FeSO4 + H2↑
56 2
x 0.9g
![]()
x=25.2g
样品中单质铁的质量分数是![]() =84%
=84%
(4)设第1次实验消耗稀硫酸中溶质的质量为y。
Fe+ H2SO4 =FeSO4 + H2↑
98 2
y 0.2g
![]()
y=9.8g
所用稀硫酸的溶质的质量分数为![]() =19.6%
=19.6%

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案