题目内容
(2013?历城区二模)如图所示为实验室中常见的气体制备、干燥、净化和收集实验的部分仪器.试根据题目要求,回答下列问题:(设过程中所有发生的反应都恰好完全进行)
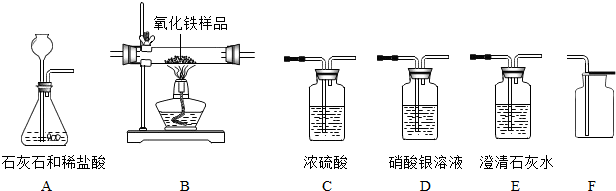
(1)用石灰石和稀盐酸为原料制取并收集干燥、纯净的二氧化碳气体.某同学设计的仪器连接顺序为:A→C→D→F.
①仪器A中发生的化学反应方程式是
②上述方案是否合理?请简述理由.
(2)欲用纯净的一氧化碳气体,测定某不纯氧化铁样品的纯度(杂质不反应),并验证反应后气体生成物的性质.某同学所选仪器的连接顺序为:一氧化碳→B→E.
①仪器B中看到的实验明显现象是
②仪器E中发生反应的化学方程式为
③通过测量反应前、后B处大玻璃管的质量变化,来计算氧化铁样品的纯度.若实验结束后大玻璃管中的物质里还有少许红色氧化铁,则计算出样品纯度的结果将
④从环境保护的角度考虑,该套实验装置存在的不足是

(1)用石灰石和稀盐酸为原料制取并收集干燥、纯净的二氧化碳气体.某同学设计的仪器连接顺序为:A→C→D→F.
①仪器A中发生的化学反应方程式是
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.②上述方案是否合理?请简述理由.
不合理,因为D排在C后,收集到的CO2气体中混有水蒸气(合理答案均可)
不合理,因为D排在C后,收集到的CO2气体中混有水蒸气(合理答案均可)
.(2)欲用纯净的一氧化碳气体,测定某不纯氧化铁样品的纯度(杂质不反应),并验证反应后气体生成物的性质.某同学所选仪器的连接顺序为:一氧化碳→B→E.
①仪器B中看到的实验明显现象是
红色粉末逐渐变为黑色
红色粉末逐渐变为黑色
.②仪器E中发生反应的化学方程式为
CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
.③通过测量反应前、后B处大玻璃管的质量变化,来计算氧化铁样品的纯度.若实验结束后大玻璃管中的物质里还有少许红色氧化铁,则计算出样品纯度的结果将
偏小
偏小
(填“偏大”、“偏小”、“不受影响”其中之一).④从环境保护的角度考虑,该套实验装置存在的不足是
没有尾气处理装置
没有尾气处理装置
,请提出你的合理建议点燃尾气或在装置末端系一只气球
点燃尾气或在装置末端系一只气球
.分析:(1)①据石灰石和稀盐酸反应原理书写方程式;
②气体从溶液中出来会带来部分水蒸气,所以干燥气体的浓硫酸通常放于最后;
(2)①一氧化碳还原氧化铁生成铁和二氧化碳,氧化铁是红色的,铁粉是黑色的;
②检验二氧化碳用澄清的石灰水,二者反应生成碳酸钙沉淀和水;
③反应前、后B处大玻璃管减少的质量即为参加反应的氧化铁中氧元素的质量,根据题意:实验结束后大玻璃管中的物质里还有少许红色氧化铁,说明氧化铁未完全反应,则减少的质量小于样品中氧化铁中氧元素的质量,故计算的样品的纯度偏小;
④一氧化碳有毒,不反应的一氧化碳要进行尾气处理,防止污染大气.
②气体从溶液中出来会带来部分水蒸气,所以干燥气体的浓硫酸通常放于最后;
(2)①一氧化碳还原氧化铁生成铁和二氧化碳,氧化铁是红色的,铁粉是黑色的;
②检验二氧化碳用澄清的石灰水,二者反应生成碳酸钙沉淀和水;
③反应前、后B处大玻璃管减少的质量即为参加反应的氧化铁中氧元素的质量,根据题意:实验结束后大玻璃管中的物质里还有少许红色氧化铁,说明氧化铁未完全反应,则减少的质量小于样品中氧化铁中氧元素的质量,故计算的样品的纯度偏小;
④一氧化碳有毒,不反应的一氧化碳要进行尾气处理,防止污染大气.
解答:解:(1)①石灰石和稀盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;
②制取并收集干燥、纯净的二氧化碳气体,可将生成的二氧化碳通入硝酸银溶液除去氯化氢气体,再通过浓硫酸进行干燥,然后收集,该同学将气体先通过浓硫酸干燥、再通过硝酸银溶液,气体从硝酸银溶液中出来时会带来水蒸气,从而使收集的二氧化碳含有水蒸气;
(2))①一氧化碳还原氧化铁生成铁和二氧化碳,氧化铁是红色的,铁粉是黑色的,故B中看到的现象是红色粉末变为红色;
②检验二氧化碳用澄清的石灰水,二者反应生成碳酸钙沉淀和水,方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;
③反应前、后B处大玻璃管减少的质量即为参加反应的氧化铁中氧元素的质量,根据题意:实验结束后大玻璃管中的物质里还有少许红色氧化铁,说明氧化铁未完全反应,则减少的质量小于样品中氧化铁中氧元素的质量,因为氧化铁的纯度=
×100%,所以,若实验结束后大玻璃管中的物质里还有少许红色氧化铁.则计算出样品纯度的结果将偏小;
④一氧化碳有毒,不反应的一氧化碳要进行尾气处理,防止污染大气,而图示没有,可以将气体点燃或在装置末端系一只气球;
故答案为:
(1)①CaCO3+2HCl=CaCl2+H2O+CO2↑;
②不合理,因为D排在C后,收集到的CO2气体中混有水蒸气(合理答案均可);
(2)①红色粉末逐渐变为黑色; ②CO2+Ca(OH)2=CaCO3↓+H2O;
③偏小; ④没有尾气处理装置;点燃尾气或在装置末端系一只气球.
②制取并收集干燥、纯净的二氧化碳气体,可将生成的二氧化碳通入硝酸银溶液除去氯化氢气体,再通过浓硫酸进行干燥,然后收集,该同学将气体先通过浓硫酸干燥、再通过硝酸银溶液,气体从硝酸银溶液中出来时会带来水蒸气,从而使收集的二氧化碳含有水蒸气;
(2))①一氧化碳还原氧化铁生成铁和二氧化碳,氧化铁是红色的,铁粉是黑色的,故B中看到的现象是红色粉末变为红色;
②检验二氧化碳用澄清的石灰水,二者反应生成碳酸钙沉淀和水,方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;
③反应前、后B处大玻璃管减少的质量即为参加反应的氧化铁中氧元素的质量,根据题意:实验结束后大玻璃管中的物质里还有少许红色氧化铁,说明氧化铁未完全反应,则减少的质量小于样品中氧化铁中氧元素的质量,因为氧化铁的纯度=
| 氧化铁质量 |
| 样品质量 |
④一氧化碳有毒,不反应的一氧化碳要进行尾气处理,防止污染大气,而图示没有,可以将气体点燃或在装置末端系一只气球;
故答案为:
(1)①CaCO3+2HCl=CaCl2+H2O+CO2↑;
②不合理,因为D排在C后,收集到的CO2气体中混有水蒸气(合理答案均可);
(2)①红色粉末逐渐变为黑色; ②CO2+Ca(OH)2=CaCO3↓+H2O;
③偏小; ④没有尾气处理装置;点燃尾气或在装置末端系一只气球.
点评:本题综合考查了常见的气体制备、干燥、净化和收集实验,一氧化碳还原氧化铁的化学反应以及相关知识的考查,要结合所学知识细心解答.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
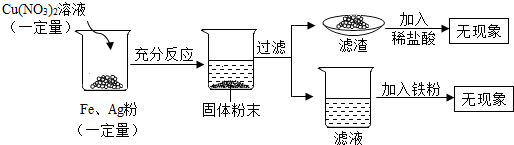
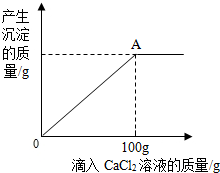 (2013?历城区二模)小丽同学利用一瓶敞口放置已久的NaOH溶液进行了一些实验探究.
(2013?历城区二模)小丽同学利用一瓶敞口放置已久的NaOH溶液进行了一些实验探究.