题目内容
【题目】下列各组物质的溶液,不用其他试剂,不能将它们一一鉴别出来的是( )
A.Ba(OH)2 NaCl Na2SO4 Na2CO3
B.NaOH Ca(OH)2 HNO3 Na2CO3
C.BaCl2 NaCl NaOH CuSO4
D.HCl CaCl2 AgNO3 Na2CO3
【答案】A
【解析】
不用其他试剂进行物质鉴别,首先观察颜色,再需要两两互相混合,观察反应现象进行鉴别;离子不能共存的条件是能生成了气体,沉淀或水。
A、四种都是无色透明溶液,两两混合,Na2CO3与Ba(OH)2生成白色沉淀BaCO3,Na2SO4 与Ba(OH)2生成白色沉淀BaSO4,其他的溶液不发生反应,无法鉴别,故符合题意;
B、四种都是无色透明溶液,四种溶液两两混合,![]() 与
与![]() 反应生成
反应生成![]() 白色沉淀,
白色沉淀,![]() 与
与![]() 反应生成
反应生成![]() 气体,四种物质能够鉴别,故不符合题意;
气体,四种物质能够鉴别,故不符合题意;
C、![]() 溶液为蓝色溶液,可以鉴别出来,然后与其他三种物质两两混合,
溶液为蓝色溶液,可以鉴别出来,然后与其他三种物质两两混合,![]() 溶液与
溶液与![]() 溶液反应有白色
溶液反应有白色![]() 沉淀生成,
沉淀生成,![]() 溶液与
溶液与![]() 溶液反应有蓝色
溶液反应有蓝色![]() 沉淀生成,四种物质能够鉴别,故不符合题意;
沉淀生成,四种物质能够鉴别,故不符合题意;
D、四种无色透明溶液,两两混合后,![]() 与
与![]() 反应生成白色
反应生成白色![]() 沉淀,
沉淀,![]() 与
与![]() 反应生成白色
反应生成白色![]() 沉淀,
沉淀,![]() 与
与![]() 反应生成白色
反应生成白色![]() 沉淀,与其他三种溶液都能产生白色沉淀,能够确定
沉淀,与其他三种溶液都能产生白色沉淀,能够确定![]() 溶液;又
溶液;又![]() 与
与![]() 反应生成白色
反应生成白色![]() 沉淀,
沉淀,![]() 与
与![]() 反应生成
反应生成![]() 气体,与其他两种溶液产生沉淀,另一种溶液生成气体,能够确定
气体,与其他两种溶液产生沉淀,另一种溶液生成气体,能够确定![]() 溶液;与
溶液;与![]() 溶液生成气体的溶液即为
溶液生成气体的溶液即为![]() ,能够鉴别,故不符合题意。
,能够鉴别,故不符合题意。
故选A。

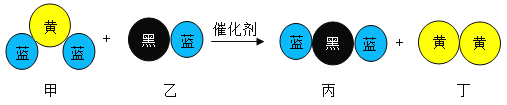
【题目】在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
物质 | W | G | H | P |
反应前质量/g | 18 | 1 | 2 | 32 |
反应后质量/g | 待测 | 26 | 2 | 12 |
关于此反应的认识不正确的是( )
A. 物质H可能是该反应的催化剂B. 该反应一定是化合反应
C. 在反应物和生成物中,G、P的质量比为4:5D. 待测值为13
【题目】化学反应有的放出热量称为放热反应,有的吸收热量称为吸热反应。化学反应有快有慢,一般增大反应物浓度、接触面积、升高温度、使用催化剂均可加快反应速率
(1)下列过程是化学变化且是放热反应的是(填编号)_____
A 浓硫酸溶于水
B 生石灰加入水中
C NH4NO3 晶体溶于水
D 天然气燃烧
E 制水煤气
(2)实验室用锌粒与 10mL30%的稀 H2SO4反应制取 H2。
①下列措施不能加快反应速率的是(填编号)_______________________。
A 加热
B 将锌粒换成锌粉
C 将 30%的 H2SO4 换成 50%的 H2SO4
D 将 30%的 H2SO4,增加到 20mL
E加入适量 Na2SO4 固体
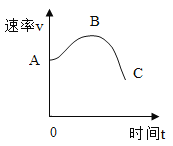
②反应速率v 随时间变化如图所示A→B 速率加快的原因是__________________________;B→C 速率减慢的原因是__________。
(3)实验室用 H2O2 制 O2,为加快反应速率常采取的措施是__________,反应方程式为_____。
(4)已知反应 Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,将一定量 Na2S2O3 溶液、稀 H2SO4 和H2O 同时混合,下列各组实验中最先出现浑浊的是(填编号)______________________。
实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O |
A | 20 | 40% 20g | 40% 20g | 10g |
B | 20 | 40% 25g | 40% 20g | 5g |
C | 40 | 80% 10g | 40% 20g | 20g |
D | 40 | 50% 10g | 60% 10g | 5g |
【题目】测定空气中氧气的体积分数可以采用下图甲乙两种装置。乙装置可视为甲的改进装置,在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化。
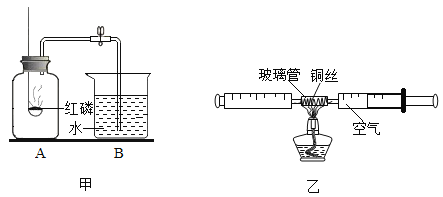
(1)在甲装置实验过程中,红磷燃烧产生大量白烟,当温度降到室温,打开止水夹,会观察到的现象是_____,写出红磷燃烧的符号表达式_____。
(2)在乙装置实验加热过程中,交替缓慢推动两个注射器活塞的目的是_____。
(3)写出乙装置实验中反应的符号表达式_____。
(4)乙装置实验中测得实验结果如下:
反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
25mL | 22mL |
由此数据可以推算出测定的空气中氧气的体积分数_____2l%(填“>”、“=”或“<”),造成该实验出现误差的原因可能是_____。(填序号)
①没有交替缓缓推动两个注射器活塞; ②读数时没有冷却至室温;
③加入铜丝量太多; ④加入铜丝量太少
(5)乙装置与甲装置相比较,优点在于_____(任答一点)。
【题目】正确分析图表信息可以帮助我们发现规律,解决问题。请你根据下列溶解度数据表与溶解度曲线图回答问题:
温度/℃ 溶解度/g 物质 | 0 | 20 | 40 | 60 | 80 | 100 |
NaCl(氯化钠) | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| 72.5 | 64 | 55 | 44.2 | 32.5 | 22 |
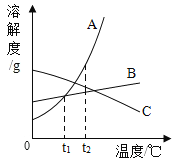
(1)A、B两种物质溶解度相等时的温度大致范围在________℃之间。
(2)![]() ℃时,A、B、C三种物质的溶解度由大到小的顺序为________________________。
℃时,A、B、C三种物质的溶解度由大到小的顺序为________________________。
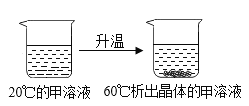
(3)如下图所示,结合上面两个图表分析,甲溶液中溶质对应的溶解度曲线应为________(填序号)。
(4)若将![]() ℃时A、B、C三种物质的饱和的溶液降温至
℃时A、B、C三种物质的饱和的溶液降温至![]() ℃时,溶液的溶质质量分数的大小顺序为__________________________________。
℃时,溶液的溶质质量分数的大小顺序为__________________________________。