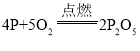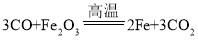题目内容
【题目】兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验,请你与他们一起完成以下探究活动。
[对固体猜想]
猜想1:全部是NaOH;猜想2:全部是Na2CO3;猜想3:__________________。
[实验和推断]

(1)若A是盐酸,现象a为有气泡产生,说明氢氧化钠已经变质。
(2)若A是Ca(OH)2溶液,现象a为白色沉淀,现象b为无色酚酞溶液变红,该实验________________ (填“能”或“不能”)说明样品中有NaOH。
(3)若A是CaCl2溶液,当实验现象a为________________,现象b为________________,则猜想2成立。
[反思]久置的氢氧化钠变质的原因是_________________(用化学方程式表示)。
【答案】Na2CO3和NaOH的混合物 不能 产生白色沉淀 无色酚酞溶液不变红色 ![]()
【解析】
对固体猜想:
氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水,如氢氧化钠未变质,则固体全部是氢氧化钠,如全部变质,则固体全部是碳酸钠,如部分变质,则固体是氢氧化钠和碳酸钠的混合物,故猜想3:Na2CO3和NaOH的混合物;
实验和推断:
(2)若A是氢氧化钙,氢氧化钙与碳酸钠反应生成碳酸钙和氢氧化钠,现象a为白色沉淀,现象b为无色酚酞溶液变红,该实验不能说明样品中有NaOH,因为反应生成的氢氧化钠也能使无色酚酞试液变红;
(3)猜想2成立,则固体全部是碳酸钠,碳酸钠与氯化钙反应生成碳酸钙和氯化钠,产生白色沉淀,氯化钠呈中性,滴入无色酚酞试液,不变色,故当实验现象a为产生白色沉淀;现象b为无色酚酞溶液不变红色,则猜想2成立;
反思:
氢氧化钠与二氧化碳反应生成碳酸钠和水,该反应的化学方程式为:![]() 。
。

【题目】分析下列表格及依据表格中部分数据绘制的溶解度曲线,下列说法中正确的是
温度/℃ | 0 | 20 | 40 | 60 | |
溶解度/g | 氯化钠 | 35.7 | 36 | 36.6 | 37.3 |
硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | |
氢氧化钙 | 0.185 | 0.165 | 0.141 | 0.116 | |
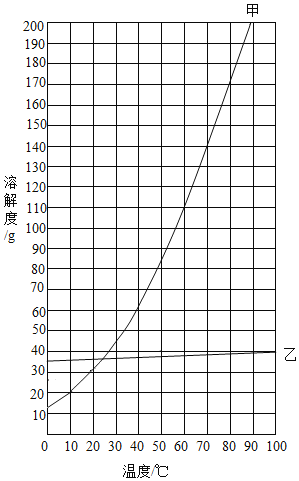
A.推测曲线甲表示氯化钠的溶解度曲线
B.20℃时,氯化钠饱和溶液中溶质的质量分数为36%
C.20℃时,硝酸钾的饱和溶液升温至60℃,溶质的质量分数变大
D.将20℃时氢氧化钙的不饱和溶液变为饱和溶液,可采取升温的方法
【题目】下列知识归纳都正确的一组是()
A 物质类型与组成 | B 化学反应基本类型 |
生铁、钢都是铁合金 纯碱、烧碱都是碱 干冰、可燃冰都是冰 | ①化合反应: ②分解反应: ③置换反应: |
C 化学反应的条件 | D 化学反应中常见的“三” |
铁生锈——与氧气或水接触 复分解反应——生成气体或沉淀或水 金属与稀硫酸反应——所有金属都可以 | ①煤、石油、天然气,三大化石燃料 ②可燃物、氧气、温度达到着火点,燃烧三条件 ③分子、原子、离子,构成物质的三种粒子 |
A.AB.BC.CD.D
【题目】控制变量,设计对比实验是实验探究的重要方法。
实验 | 一、探究人体呼出气体中二氧化碳含量比空气中的高 | 二、探究影响品红扩散快慢的因素 | 三、铁钉锈蚀条件的探究 |
实验 |
|
|
|
实验 | 本实验条件除了要控制两个盛装气体样品的集气瓶大小规格相同外,还要控制 相同。 | 发现两杯水都变红,且整杯热水变红时间比冷水要短。由此说明:①分子在不断运动;②影响分子运动快慢的因素有 。 | 一周后,左边试管中铁钉生锈,右边试管中铁钉无明显变化。上述实验 |