题目内容
【题目】小明在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究。
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】①6H2SO4(浓)+2Fe ![]() Fe2(SO4)3+6 H2O +3SO2↑
Fe2(SO4)3+6 H2O +3SO2↑
②SO2可使品红溶液的红色褪去。
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫。
(1)【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验。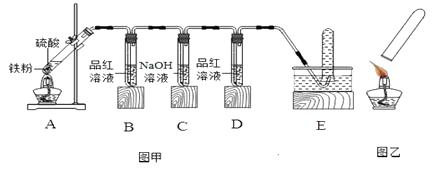
请帮助小明完成下表:
A中硫 | 实验现象 | A中生成气体成分 | |||
B中品 | D中品 | 爆鸣实验 | |||
实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | |
实验三 | 25% | 不褪色 | 只有H2 | ||
【实验结论】铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸浓度达到足够大时,生成的气体产物中有二氧化硫。
(2)【交流反思】①写出实验三中铁与硫酸反应的化学方程式:。
②实验一中C装置中反应的化学方程式:。
(3)【拓展延伸】在初中化学教材中也有反应物浓度不同,生成的产物不同的例子
【答案】
(1)有SO2 和H2;不褪色;有爆鸣声
(2)Fe+H2SO4=FeSO4+H2↑;2NaOH+SO2=Na2SO3+H2O
(3)碳在氧气充足时生成二氧化碳不充足时生成一氧化碳
【解析】 (1)由题中叙述可知,实验中的现象为
A中硫 | 实验现象 | A中生成气体成分 | |||
B中品 | D中品 | 爆鸣实验 | |||
实验一 | |||||
实验二 | 有SO2 和H2 | ||||
实验三 | 不褪色 | 有爆鸣声 | |||
(2)【交流反思】①实验三中铁与硫酸反应的化学方程式:Fe+H2SO4=FeSO4+H2↑,②实验一中C装置中反应的化学方程式2NaOH+SO2=Na2SO3+H2O;
(3)【拓展延伸】反应物浓度不同,生成的产物不同的例子为碳在氧气充足时生成二氧化碳不充足时生成一氧化碳.
故答案为:(1)有SO2 和H2;不褪色;有爆鸣声;(2)Fe+H2SO4=FeSO4+H2↑;2NaOH+SO2=Na2SO3+H2O;(3)碳在氧气充足时生成二氧化碳不充足时生成一氧化碳.
(1)A中生成气体成分可能只有SO2和H2中的一种,也可能是二者的混合物,SO2能使品红褪色,氢气做爆鸣实验时有爆鸣声;
(2)铁和硫酸反应生成硫酸亚铁和氢气,氢氧化钠和二氧化硫反应生成亚硫酸钠和水;
(3)碳在完全燃烧和不完全燃烧的条件下的产物是不同的.

 出彩同步大试卷系列答案
出彩同步大试卷系列答案【题目】石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
稀盐酸的用量 | 5g | 5g | 5g | 5g |
剩余固体的质量 | 3g | 2g | 1g | 1g |
(1)该石灰石样品中碳酸钙的质量分数是;
(2)计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%).
(3)第三次加入5g稀盐酸后所得溶液的质量为 。