题目内容
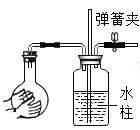
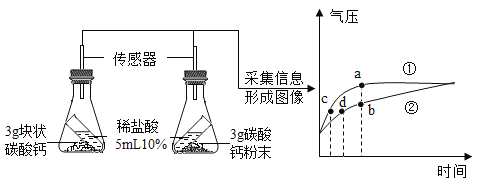
【题目】利用传感器技术可以形象地比较不同形状的碳酸钙和稀盐酸反应的速率。某同学倾斜锥形瓶,使试管内的稀盐酸流入瓶中与碳酸钙发生反应,测得瓶内气压随时间的变化如图所示。
(1)写出碳酸钙与稀盐酸反应的化学方程式:_____。
(2)下列有关说法正确的是_____(填字母序号)。
A 对比分析a、b点可知,曲线①表示块状碳酸钙与稀盐酸的反应
B 通过实验可知,实验室制取二氧化碳应该选用碳酸钙粉末与稀盐酸
C 对比分析c、d点可知,相同气压时,碳酸钙粉末与稀盐酸反应的速率更快
D 碳酸钙粉末与稀盐酸反应产生的二氧化碳更多
【答案】CaCO3+2HCl=CaCl2+H2O+CO2↑ C
【解析】
(1)碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑。
(2)A.对比分析a、b点可知,曲线①单位时间内气压大,说明单位时间内产生的气体多,反应速率快,曲线①表示粉末状碳酸钙与稀盐酸反应,错误。
B.实验室不选用石灰石粉末制取二氧化碳的理由是:反应速率太快,不利于二氧化碳的收集,故错误。
C.最终曲线①、②的气压相等,说明最终产生的CO2质量相等,故错误。
故答案为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑;(2)C。

练习册系列答案
相关题目