题目内容
【题目】A~E 是初中常见的物质,它们的转化关系如图所示(图中“→”代表转化,“—”代表反应)B 可用于补钙,A和B属于同类别物质,C 和E属于另一种同类别物质。请回答:
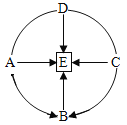
(1)B的化学式为___________;
(2)A和D反应的化学方程式为______________________。
【答案】CaCO3 ![]() 或
或![]() (答案不唯一)
(答案不唯一)
【解析】
根据题意,B可用于补钙,则推测B为CaCO3;又A、B为同类别物质,故A为盐类物质,且A能转化为B,推测A为可溶性碳酸盐;由B能转化为E,推测E可能为水或二氧化碳;又C 、E为同类别物质,即C也为氧化物,且C能转化为E,因为二氧化碳与氢氧化钠反应能生成水,但是水不能转化为二氧化碳,故推测C为CO2,E为H2O;D既能和A反应,又能和C反应,即D能和碳酸盐反应,也能和CO2反应,则D应为Ca(OH)2或Ba(OH)2。
(1) B 可用于补钙,则推测B为CaCO3;故填:CaCO3;
(2)A为可溶性碳酸盐,即可以是Na2CO3或K2CO3等,D为Ca(OH)2或Ba(OH)2,此题答案不唯一,可填:![]() 或
或![]() 。
。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】同学们在整理实验室时,发现一包白色粉末状药品,老师说该药品由氯化钠、碳酸钙、氢氧化钠中的两种组成,同学们对此很好奇,于是对这包白色粉末的成分进行如下探究。
(作出猜想)猜想一:_______ 猜想二:CaCO3和NaOH 猜想三:NaCl和NaOH
(设计实验)
实验步骤 | 实验现象 | 实验结论 |
(1)取一定量白色粉末于烧杯中,加足量水,搅拌 | ________ | 猜想三不成立 |
(2)取少量(1)中所得溶液于试管中,向其中滴入氯化铜溶液 | ________ | 猜想二不成立 |
(3)另取少量(1)中所得溶液于试管中,向其中滴加过量的____溶液 | 产生白色沉淀 | 猜想一成立 |
写出步骤(3)中发生反应的化学方程式____。
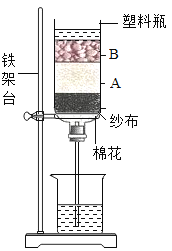
(拓展延伸)如何测定该白色粉末中碳酸钙的质量分数呢?某同学利用碳酸钙能与稀盐酸反应产生二氧化碳来测定该白色粉末中碳酸钙的质量分数,利用下列装置测定二氧化碳的质量。
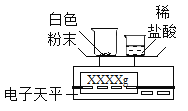
(1)将小烧杯中的所有稀盐酸分几次加入到大烧杯中并不断搅拌,判断白色粉末中碳酸钙完全反应的实验现象是_____。
(2)已知反应前的总质量[m(大烧杯+白色粉末)+m(小烧杯+稀盐酸)],要计算生成CO2的质量,至少还需要的数据是____(填序号)。
A m(小烧杯) B m(大烧杯) C m(大烧杯+反应后剩余物)